
7.若ⅢA族某元素的原子序数为m,则原子序数为m – 1的元素 ( )
A.一定是第ⅡA族元素 B.一定是第ⅡB族元素
C.可能是第ⅡA族或第ⅡB族元素 D.可能是第ⅤⅢ族元素
5.下列各选项中,两个反应所遵循的化学原理最相似的是 ( )
A.葡萄糖和甲醛分别与新制的氢氧化铜悬浊液共热,都产生红色沉淀
B.苯酚和乙烯都能使溴水褪色
C.二氧化硫和过氧化氢都使品红溶液褪色
D.氯气用于水的杀菌消毒和明矾用于净水
|
A.FeSO4 B.K2SO4 C.AlCl3 D.NH4HCO3
4. 由于反应条件的改变使某容器中的平衡mA(g) + nB(g) pC(g);△H<0向正反应方程发生了移动。新的平衡状与原平衡状态相比,下列判断正确的是 ( )
由于反应条件的改变使某容器中的平衡mA(g) + nB(g) pC(g);△H<0向正反应方程发生了移动。新的平衡状与原平衡状态相比,下列判断正确的是 ( )
A.容器内的温度一定升高 B.正反应速率可能变大,也可能变小
C.容器中C物质的浓度一定升高 D.容器中B物质的浓度一定降低
3.目前,人类已经发现的非金属元素除稀有气体元素外共有16种,下列对这16种非金属元素的判断正确的有 ( )
①都是主族元素,最外层电子数都大于3
②单质形成的晶体都为分子晶体
③氢化物常温下都是气态,所以又叫做气态氢化物
④氧化物常温下都可以与水反应生成酸
A.只有①②正确 B.只有①③正确
C.只有③④正确 D.①~④都不正确
2.NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.1mol P4中含P-P共价键4NA
B.用惰性电极电解CuSO4溶液时,当电路中通过1mole-时,溶液中产生的H+数目为NA
C.1molC5H12中单键数目为12NA
D.常温常压下,1mol任何气体所含原子数目都为NA
1.下列反应:①Na + H2O ②Na2O + H2O ③NO2 + H2O ④Cl2 + H2O ⑤F2 + H2O
⑥SO2 + H2O中,属于氧化还原反应,但水既不是氧化剂,又不是还原剂的是 ( )
A.①③ B.②⑥ C.③④ D.④⑤
23.(10分)某学生为了测定某种稀硫酸的物质的量浓度,用不同质量的纯锌粉与该稀硫酸进行反应。他的六次实验结果如下(计算结果精确到0.1):
|
实验编号 |
加入锌粉的质量(g) |
稀硫酸溶液的体积(mL) |
生成硫酸锌的质量(g) |
|
1 |
2.0 |
50.0 |
5.0 |
|
2 |
4.0 |
50.0 |
|
|
3 |
6.0 |
50.0 |
14.9 |
|
4 |
8.0 |
50.0 |
19.3 |
|
5 |
10.0 |
50.0 |
|
|
6 |
12.0 |
50.0 |
19.3 |
(1)其中第2、第5两个实验中生成硫酸锌的质量分别是 g、 g。
(2)在右图中画出生成硫酸锌的质量[m(ZnSO4)]与加入锌粉质量[m(Zn)]的关系示意图(需要标明关键点的横坐标和纵坐标的数据)。
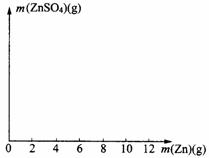
(3)若使(10+m)g锌粉与50.0mL上述稀硫酸充分反应,剩余固体的质量为_______g,该稀硫酸的物质的量浓度为______mol/L。
22. (10分)有如下化学反应:2A(g)+B(g)
2C(g)(△H<0)
(10分)有如下化学反应:2A(g)+B(g)
2C(g)(△H<0)
(1)若将4mol气体A和2mol气体B在2L密闭容器中混合,经2s后测得C的浓度为0.6mol·L-1。则2秒时B的浓度为 mol·L-1。
(2)若把amol气体A和b mol气体B充入上述密闭容器,达到平衡时,它们的物质的量满足n(A)+n(B)=n(C),则气体A的转化率为 。
(3)如下图所示,将4mol气体A和2mol气体B混合后置于体积可变的等压容器中,一定温度下达到平衡状态X时,测得气体总物质的量为4.2mol。若A、B、C起始的物质的量分别用a、b、c表示,试回答: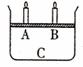
①达到平衡状态X时的容器中,通入少量B气体,容器中A的体积分数 (填“增大”、“减小”或“不变”)。若要使A的体积分数再升高到与平衡状态X相同,可采取的一种措施是 (只填一种即可)。
②若起始a=1.2mol,b=0.6mol,且达到平衡后各气体的体积分数与平衡状态X相同,则起始时C的取值范围为 。
21.(10分)下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。(b)反应①、②是化工生产中的重要反应。(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。(e)化合物J由两种元素组成,其相对分子质量为32。
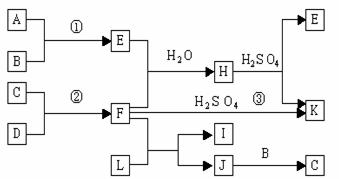
请按要求填空:
(1)反应③的化学方程 。
(2)C的结构式 ;H的化学式 。
(3)L的溶液与化合物E反应的离子方程式 。
(4)化合物J的化学式 。
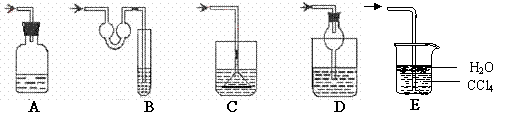
20.(8分)(1)以下各种尾气吸收装置中,适合于吸收HCl气体,而且能防止倒吸的有
__________

(2)现用物质的量的浓度为a mol / L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
①酸式滴定管用蒸馏水洗净后,还应该进行的操作是 ;
②下图是酸式滴定管中液面在滴定前后的读数:


c(NaOH)= ;
③若在滴定前滴定管尖嘴部分有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度会偏 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com