
6、NA代表阿伏加德罗常数,下列说法正确的是( )
A.0.5 mol Al与足量盐酸反应转移电子数为1NA
B.标准状况下,11.2 L SO3所含的分子数为0.5NA
C. 0.1 mol CH4所含的电子数为1NA
D.46 g NO2和N2O4的混合物含有的分子数为1NA
5、KNO3的溶解度在80℃时为mg,20℃时为ng,20℃时饱和溶液中KNO3的质量分数为p%,则下列数据关系正确的是 ( )
A.m<n<p B.m>n>p C.n>m>p D.p>m>n
4、下列实验中,①配制-定物质的量浓度的溶液 ②pH试纸的使用 ③过滤 ④蒸发
⑤溶解,均用到的仪器是 ( )
A.烧杯 B.漏斗 C.玻璃棒 D.胶头滴管
3、关于Na2O和Na2O2的叙述正确的是 ( )
A.都是白色的固体 B.都是碱性氧化物
C.都能和水反应形成强碱溶液 D.都是强氧化剂
2、下列离于方程式正确的是( )
A.钠与水反应:Na +2H2O = Na+ + 2OH- + H2↑
B.往碳酸氢钙溶液中加过量烧碱:HCO3-+OH- = CO32-+H2O
C.用醋酸中和氢氧化钠溶液:H++OH- = H2O
D.将饱和氯化铁溶液滴入沸水中:Fe3++3H2O==Fe(OH)3(胶体)+3H+
1、下列物质久置于敞口容器中,不易变质的是( )
A.漂白粉 B.苯酚 C.碳酸钠 D.氧化钙
12、(15分)氮气和氢气在一定条件下在一密闭容器中发生如下反应:
N2(g)+3H2
(g) 2NH3(g)+Q (Q>O)
2NH3(g)+Q (Q>O)
(!)写出该反应的化学平衡常数表达式___________________(3分)
(2)升高温度,该反应的K值________(2分),化学反应速率_______(2分),氨气的百分含量____________(2分)。(以上均填增大、减小或不变)
(3)下图表示上述反应在某一时间段中反应速率与反应过程的关系图。由图判断,氨的百分含量最高的一段时间是____________(2分)。

(4)据图判断反应在t2-t3这段时间内,曲线变化的原因是____________(2分)(用文字表达),t5~t6时间内曲线变化的原因可能是_________(2分)(填写编号)
(a) 加了催化剂 (b) 扩大容器的体积 (c) 降低温度 (d) 增加了NH3的量
13(15分)下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝且X加热分解生成A和C的体积相同。
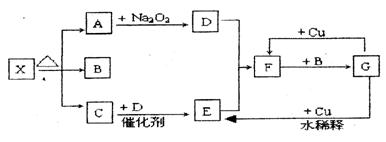
(1)写出下列各物质的化学式:
X: ;B: ;F: ;
(2)写出下列变化的反应方程式,是离子反应的只写其离子方程式:
C→E: ;
G→E: 。
(3)实验室制取C气体后,试管内残余的气体最好用蘸有_______ (填 “H2O”“稀硫酸”“浓NaOH溶液”“浓盐酸”)的棉球吸收以防止污染。
(4)又知G的浓溶液和足量的Cu充分反应,若产生的气体与1.12L(标准状况)O2混合后通入水中,恰好被吸收,则溶解的Cu的质量为_________g。(3分)
14(10分)、向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(气)+ 3 H2(气) 2 NH3(气),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(气),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
①.若a=0,b=0,则c= .
②.若a=0.7,b=2.1,则:
Ⅰ.c= .
Ⅱ.这时反应向 进行.
Ⅲ.若要维持反应开始向该反应方向进行,c的范围是 .
③.欲使起始反应维持向与②相反的方向进行,则b的范围是
11、(10分)下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。

请按要求填空:
⑴G的电子式是_____________(2分);
⑵反应⑥的化学方程式是_______________________________(2分),反应⑤在空气中发生时的现象是_____________________________(2分),已知C的燃烧热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是 ______________________________(2分)。
⑶根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是__________(2分)。
10、两份质量为m的硫,分别跟足量的氢气和氧气反应,反应后将生成物混合,析出硫的质量( )
A.2m B.1m C.1.5m D.0.5
9、为了除去NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理(反应方程式:3NO2 + 2NaOH→2NaNO3 + NO + H2O;NO2 + NO + 2NaOH→2NaNO2)。现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体恰好被V L NaOH(aq)吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度为 ( )
A. mol/L
B.
mol/L
B. mol/L
mol/L
C.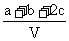 mol/L
D.
mol/L
D. mol/L
mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com