
20.(13分)为测定氢氧化钠和碳酸钠固体混合物样品中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
I.甲同学的方案是:将m g样品溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称得固体n g。
(1)混合物中碳酸钠的质量分数为(用m、n表示)_______________________
甲同学洗涤沉淀的具体操作是_______________________________________
 (2)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是①______________________ ;②BaCO3的摩尔质量比CaCO3的大,相同质量的Na2CO3,产生沉淀的质量大,称量误差小。
(2)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是①______________________ ;②BaCO3的摩尔质量比CaCO3的大,相同质量的Na2CO3,产生沉淀的质量大,称量误差小。
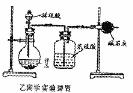
Ⅱ.乙同学的方案如右图:
(1)盛有浓硫酸的装置的作用为_____________________
(2)乙同学的方案的装置中存在一定的缺陷,请你提出改进的方法(简单叙述做法,不必画图)_______________________________________________
19.(7分)如下图所示,A可用作实验室制取气体的发生装置,B、C、D为常见仪器。请回答下列问题:
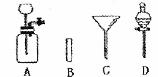
(1)仪器D的名称是_________,列举C的一种常见用途为_____________。
(2)用本题中的A装置(气密性良好)制取气体时,常会有生成的气体逸散到空气中,有的还会造成污染。为避免上述弊端,请在B、C、D中选择适当的仪器,对A进行重新设计和组装。(以简洁的文字予以说明)
安装方法①_____________________________________________。
安装方法②_____________________________________________。
18.如图所示,分别挤压装有液体的胶头滴管a,将液体加入到广口瓶(装有另一种物质)中,两装置中原来干瘪的气球b都有明显地胀大(忽略液体体积对气球影响)。则所用试剂中,两装置中原来干瘪的气球b都有明显地胀大(忽略液体体积对气球影响)。则所用试剂不可能是
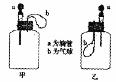 A.甲:H20和固体CaO; 乙:H20和N02
A.甲:H20和固体CaO; 乙:H20和N02
B.甲:盐酸和固体Na2O2; 乙:亚硫酸钠溶液和氯气
C.甲:NaOH溶液和C02; 乙:盐酸和NaHCO3溶液
D.甲:浓氨水和固体NaOH;乙:稀H2S04和NH3
第Ⅱ卷非选择题(必做54分+选做10分,共64分)
[必做部分]
17.已知下列热化学方程式:
(1)Fe203(s)+3CO(g)=2Fe(s)+3C02(g) △H=-25kJ·mol-1
(2)3Fe203(s)+CO(g)=2Fe304(sJ+C02(g) △H=-47kJ·mol-1
则Fe3O4(s)被CO还原成Fe和CO2的热化学方程式正确的是
A.Fe304+4CO=3Fe+4C02 △H=-14kJ·mol-1
B.Fe304(s)+4CO(g)=3Fe(s)+4C02(g) △H=-22kJ·mol-1
c. Fe304(s)+4CO(g)=3Fe(s)+4C02(g) △H=+14kJ·mol-1
D.Fe304(s)+4CO(g)=3Fe(s)+4C02(g) △H=-14kJ·mol-1
16.某化学兴趣小组欲研究H2SO4、NaCl、KCl、Na2CO3、FeCl3、NaOH的性质,对于如何研究,他们设计了两种研究方案:
方案①:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验;
方案②:将它们按照钠盐、钾盐、铁盐和其它化合物分类,然后分别溶于水得到溶液,进行实验。下列说法正确的是
A.设计方案②的同学取某种溶液,在其中加入上述的钾盐溶液有白色沉淀产生,加入稀硝酸溶液沉淀不消失,则该溶液中一定含有Ag+
B,将少量铝粉分别投入上述溶液中,按照方案①能够完全溶解铝粉的只有酸(H2SO4)溶液和盐(FeCl3)溶液
C.按照方案①属于碱的有Na2CO3、NaOH
D.这两组同学在研究物质性质时只使用了实验法、观察法
15.常温下,pH=11的氨水和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,则下列说法不正确的是
A.氨水的浓度大于盐酸的浓度
B.反应后的溶液呈酸性
C.原氨水中有1%的含氮微粒为NH4+
D.反应后的溶液中NH4+、NH3·H2O与NH3三种粒子的平衡浓度之和为0.05mol·L-1
14.已知NaHS03显酸性,NaHCO3溶液显碱性,现有浓度为0.1 mo|·L-1的NaHSO3和NaHCO3两种溶液,下列各粒子的物质的量浓度关系在两种溶液中(R表示S或C)都正确的是
A.c(Na+)>c(HR03-)>c(H+)>c(R032-)>c(OH-)
B.c(Na+)+c(H+)=c(HR03-)+c(R032-)+c(OH-)
C.c(H+)+c(H2R03)=c(R032-)+c(OH-)
D.c(Na+)=c(HR03-)+c(H2R03)+2c(R032-)
13.在下述条件下,一定能大量共存的离子组是
A.无色透明的水溶液中:K+、Mg2+、I-、MnO4-
B.pH=1的NaN03水溶液中:NH4+、Fe2+、S042-、Cl-
C.c(HC03-)=0.1mol·L-1的溶液中:Na+、K+、C032-、Br-
D.由水电离产生的c(OH-)=1×10-13mol·L-1的溶液中:H+、Al3+、Cl-、NO3-
12.巴豆酸的结构简式为CH3-CH=CH-COOH 现有①氯化氢②溴水③烧碱溶液④乙醇⑤酸性高锰酸钾溶液,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是
A.只有②④⑤ B.只有①③④ C.只有①②③④ D. ①②③④⑤
11.下列现象中,不是因为发生化学反应而产生的是
A.乙烯使酸性KMnO4溶液退色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使溴的四氯化碳溶液退色
D.甲烷与氯气混合,光照一段时间后黄绿色消失
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com