
16.将pH=3的盐酸a L分别与下列三种溶液混合后,溶液均呈中性:
① 1×10-3 mol·L-1的氨水b L
② c(OH-)=1×10-3 mol·L-1的氨水c L
③ c(OH-)=1×10-3 mol·L-1的Ba(OH)2溶液d L
其中a、b、c、d的关系正确的是
A.b>a>d>c B.b>a=d>c
C.a=b>c>d D.c>a=d>b
第Ⅱ卷(非选择题 共60分)
15.某MCFC型燃料电池可同时供应电和水蒸汽,其工作温度为600℃-700℃,所用燃料为氢气,电解质为熔融的K2CO3。该电池的总反应为:2H2+O2=2H2O,负极电极反应式为:
H2+CO32-  H2O+CO2+2e-。则下列判断中正确的是
H2O+CO2+2e-。则下列判断中正确的是
A.放电时CO32-向负极移动
B.放电时CO32-向正极移动
C.正极反应: 4OH- 2H2O+O2↑+4e-
2H2O+O2↑+4e-
D.当电池中生成1 mol水时,转移4 mol电子
14.氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成。则下列叙述不正确的是:
A.NH4H是离子化合物
B.NH4H固体投入少量的水中,有两种气体生成
C.NH4H与水反应时,NH4H是还原剂
D.NH4H溶于水,所形成的溶液显酸性
13.实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是
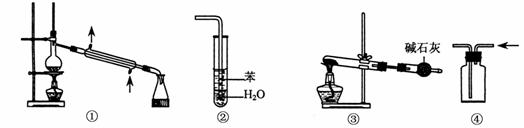
A.装置①常用于分离互不相溶的液体混合物
B.装置②可用于吸收HCl气体,并防止倒吸
C.以NH4HCO3为原料,装置③可用于实验室制备少量NH3
D.装置④可收集CO2、H2等气体
12.一定温度下,在2L的密闭容器中加入4 mol A和6 mol B,发生如下反应:2A(g)+3B(g)
4C(g)+D(g),反应10 min后达到平衡,此时D的浓度是0.5 mol·L-1。下列说法正确的是
A.反应达平衡时c(B)=1.5 mol·L-1
B.前10 min内反应的平均速率υ(C)=0.1 mol·(L·min)-1
C.恒温下,将压强变为原来的2倍,则再次达平衡时D的浓度小于1 mol·L-1
D.10 min后向容器中加入A,再次达平衡时,A的转化率一定大于50%
11.25℃时,由水电离出的氢离子浓度c(H+)=1×10-13 mol·L-1的溶液中,一定不能大量共存的离子组是
A.Cl-、[Al(OH)4]-、Na+、K+ B.Fe3+、K+、NO3-、MnO4-
C.Fe2+、Ba2+、NO3-、Cl- D.SO42-、Cl-、Na+、K+
10.下列说法中正确的是
A.同分异构体分子量相同,结构不同,化学性质一定相似
B.可以用新制的Cu(OH)2悬浊液检验患者的尿液中是否含糖
C.向鸡蛋清溶液中加入(NH4)2SO4饱和溶液,有沉淀析出,再加水沉淀不溶解
D.油脂、糖类和蛋白质是食物含有的主要营养物质,他们是高分子化合物
9.甲、乙、丙都是短周期元素,其中甲、乙两元素原子的最外层电子数分别是次外层电子数的2倍和3倍,丙元素原子K层和M层电子数之和与L层的电子数相同。则下列判断不正确的是
A.乙元素的族序数比甲元素的族序数大
B.甲、丙元素最高价氧化物对应水化物的酸性强弱顺序为:甲<丙
C.原子半径由大到小的顺序为:丙>甲>乙
D.含乙元素的化合物数目比含甲或丙元素的化合物数目多
8.元素的性质包含金属性和非金属性,其强弱可以通过该元素对应的某些化学性质体现出来。某同学认为铝元素是金属元素,但是有一定的非金属性。下列化学反应中,你认为能支持该同学观点的是
A.铝片与盐酸反应生成氢气 B.氢氧化铝溶于强碱溶液
C.氢氧化铝溶于强酸溶液 D.铝热反应
7.阿伏加德罗常数约为6.02×1023 mol-1,下列说法中一定正确的是
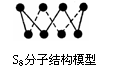 A.32 g S8单质中含有的S-S键个数为6.02×1023
A.32 g S8单质中含有的S-S键个数为6.02×1023
B.Na2O2与H2O反应生成1.12 L O2(标准状况),反应中转移的电子数
为2×6.02×1022
C.1.0 L 1.0 mol·L-1 CH3COOH溶液中,CH3COOH分子个数为6.02×1023
D.22.4 L N2中所含的分子个数为6.02×1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com