
6.将SO2气体通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体仍无沉淀产生。则通入的该气体可能是
A.CO2 B.NH3 C.NO2 D.Cl2
5.化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是
A.定性检验SO32-,将BaCl2溶液用HNO3酸化
B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C.检验溶液中是否含有Fe2+时,用硝酸酸化
D.检验溶液中是否含有SO42-时,在无其它阳离子干扰的条件下,用盐酸酸化的BaCl2溶液
4. 向氢氧化钠溶液中滴加几滴下列金属盐溶液,一定能得到白色沉淀的是
A.Al2(SO4)3溶液 B.CaCl2溶液 C.FeCl2溶液 D.MgSO4溶液
3.设NA表示阿伏加德罗常数,下列说法正确的是
A.1L1mol/L CH3COONa溶液中存在NA个CH3COO-离子
B.1molCnH2n+2含有(3n+1) NA个共价键
C.1molCl2参加化学反应获得的电子数都是2 NA
D.1molNO2气体降温后颜色变浅,其所含的分子数仍为NA
2.下列关于原子的几种描述中,错误的是
A.18O与19F具有相同的中子数 B.16O与17O具有相同的电子数
C.12C与13C具有相同的质量数 D.15N与14N具有相同的质子数
1.下列各项中表达正确的是
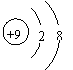

A.F-的结构示意图: B.乙炔的分子模型示意图:
C.NaCl的电子式: D.乙酸的结构简式:C2H4O2
D.乙酸的结构简式:C2H4O2
28.(l0分)卤代烃在碱性醇溶液中能发生消去反应。例如
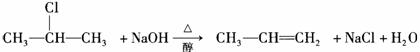
该反应式也可表示为
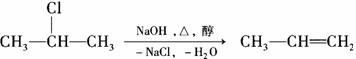
下面是八个有机化合物的转换关系

请回答下列问题:
(1)根据系统命名法,化合物A的名称是 。
(2)上述框图中,①是 反应,③是 反应。(填反应类别)
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式
。
(4)C2的结构简式是 。F1的结构简式是 。
F1和F2互为 。
(5)上述八个化合物中,属于二烯烃的是 。二烯烃的通式是 。
26.(8分)煤粉在隔绝空气中加强热,除主要得到焦炭外,还能得到下表所列的物质:
|
序号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
名称 |
甲烷 |
一氧化碳 |
乙烯 |
苯 |
甲苯 |
苯酚 |
氨水 |
(1)表中所列物质不属于有机物的是(填序号): 。
(2)能使溴水褪色的是(填序号): 。
(3)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号) ,该物质发生加聚反应的化学方程式为: 。
(4)能使氯化铁溶液变为紫色的是(填序号): 。
(5)甲苯的一氯取代产物的有 种。
 27.(12分)已知-NH2连在苯环上显碱性 连在苯环上显中性,化学式为C7H7NO2的有机物中其分子结构中有一个苯环,两个侧链(间位),符合下列条件的结构简式为:
27.(12分)已知-NH2连在苯环上显碱性 连在苯环上显中性,化学式为C7H7NO2的有机物中其分子结构中有一个苯环,两个侧链(间位),符合下列条件的结构简式为:
(1)既有酸性又有碱性 ;
(2)只有酸性 ;
(3)只有碱性 ;
(4)显中性 。

(5)由于-COOH能跟-NH2形成 ,所以可用乙二醇、对苯二甲酸跟上述既显酸性又显碱性的物质发生反应,生成高分子化合物[(C17H13NO5)]。该化合物为高强度纤维材料,其结构简式为 。 生成该物质的反应是 反应。
25.(8分)下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。
|
a |
|
b |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
c |
d |
|
|
|
|
e |
|
f |
|
|
|
g |
h |
||||||||||
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
j |
⑴i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图_________。
⑵以上元素形成的金属单质中,熔点最低的是____ (填元素符号)。
⑶NH3·H2O的电离方程式为NH3·H2O NH4++OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是______。(填序号)
NH4++OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是______。(填序号)

⑷1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是______。(填写元素符号)
⑸利用稀有气体化合物,人们实现了许多制备实验上的突破。如XeO3在一定条件下与NaBrO3反应生成NaBrO4,同时放出Xe。写出上述反应方程式:
_______________________________________________________。
24.(8分)将2 mol SO2和1 mol O2混合置于体积可变的密闭容器中,在T1温度下发生如下反应:
2SO2(g)+O2(g) 2SO3(g)
;△H<0
2SO3(g)
;△H<0
 当反应进行到时间t0点时达到平衡状态,测得混合气体的总物质的量为2.1 mol。试回答:
当反应进行到时间t0点时达到平衡状态,测得混合气体的总物质的量为2.1 mol。试回答:
(1)该反应的平衡常数表达式: 。
(2)反应进行到t0时SO2的的体积分数 。
(3)若保持温度为不变,使用催化剂,在图中作出
从反应开始到t0点这段时间SO2物质的量变化曲线。
(4)当反应进行到t1时间时(t1 >t0),给上述反应容器加热到温度为T2 (T2>T1),反应在t2 时间时(t2>t1)重
新达到平衡状 态,新平衡混合物中气体的总物质的量 ______2.1 mol(填“<”、“>”或“=”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com