
8.关于电解质的导电性,下列说法正确的是
A.与溶液中的离子浓度有关
B.与金属导电没有本质区别
C.强电解质溶液的导电能力强于弱电解质溶液的导电能力
D.导电性强的溶液中,自由移动的离子数目一定比导电性弱的溶液中自由移动的离子数目多
7.下列说法正确的是
A.32g O2占有的体积约为22.4L
B.22.4L N2含有阿伏加德罗常数个氮分子
C.在标准状况下,22.4L水的质量约为18g
D.22g CO2与标准状况下11.2L HCl含有相同的分子数
6.关于氯水的叙述中不正确的是
A.新制氯水的氧化性强于久置的氯水
B.新制氯水的pH小于久置的氯水
C.新制氯水中Cl2的分子数目多于久置的氯水
D.氯水用于漂白体现了HClO的强氧化性
5.下列反应中,属于氧化还原反应的是
①Na2O2+2HCl=2NaCl+H2O2 ②2Na2O2+2H2O=4NaOH+O2↑
③C10+H20=HCI+HCIO ④ICI+H2O=HCl+HIO
A.①④ B.①③ C.②③ D.只有②
4.下列离子方程式书写正确的是
A.石灰石与盐酸反应 CO32- +2H+=H2O+CO2↑
B.醋酸与烧碱溶液反应 H++OH-=H2O
C.氧化铜与盐酸反应 O2-+2H+=H2O
D.硫酸与氨水混合 H++NH3·H2O=NH4++H2O
3.下列物质属于非电解质的是
A.CO2 B.H2O C.Cl2 D.CH3COOH
2.某婴儿配方奶粉部分营养成分的含量如下表所示:
|
营养成分 |
钙 |
磷 |
铁 |
锌 |
|
含量/(mg/100g) |
600 |
520 |
6-11 |
3-7 |
表中的“钙、磷、铁、锌”应理解为
A.金属 B.非金属 C.元素 D.分子
1.下列说法正确的是
A.化学是科学家研究的内容,与普通百姓的生活没有多大关系
B.化学研究只能认识分子,不能创造分子
C.化学家可以制造出自然界中不存在的物质
D.化学研究只会造成严重的环境污染,最终人类将毁灭在化学物质中
29.(17分)已知:醛在一定条件下可以相互加成,例:(R1、R2代表烃基或氢原子)

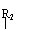
R1CHO+R2 CH2CHO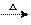 R1-CH-CHCHO R1-CH=C-CHO
R1-CH-CHCHO R1-CH=C-CHO
X的分子式是C7H6O,X能发生银镜反应,1 mol X与H2反应,消耗H2的物质的量最多为4mol,G为高分子化合物,分子式为(C9H8O2)n。已知下列反应图式中各有机化合物之间的关系(所有无机产物均已略去):
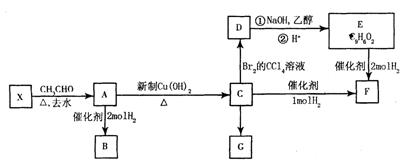
(1)写出E中官能团的名称:______________。
(2)写出下列物质的结构简式:
X是_________;A是________;G是_________。
(3)D转化为E的反应中条件①所涉及的反应类型有_______、________。
(4)写出F与B反应的化学方程式:
_______________________________________________________________________
(5)C为肉桂酸,可用于制备感光高分子材料。肉桂酸有多种同分异构体,其中含有苯环且苯环上只有一个链状取代基并属于酯类的有:

还有两种的结构简式:_______________、_____________________。
28.(17分)乙二酸具有热分解性和还原性。
I.甲同学欲设计实验证明乙二酸热分解反应的产物,并利用反应产生的CO来还原Fe2O3。
已知:HOOC-COOH(乙二酸) 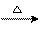 CO↑+CO2↑+H2O请回答下列问题:
CO↑+CO2↑+H2O请回答下列问题:
(1)实验所需的仪器装置如图所示:

若按气流方向从左到右,每个装置都用到而且只能用一次,连接成一套实验装置。则各仪器的连接顺序是(填各接口数字序号).____接____、_____接_____、_____接_____、_____接_____、______接_____
(2)该同学进行了下列实验操作:
a.点燃C处的酒精灯;
b.检查实验装置的气密性并装入药品;
c.反应结束后,先熄灭C处酒精灯,继续通入气体直到C中固体冷却后,再熄灭D处酒精灯;
d.点燃D处的酒精灯,开始反应,在装置的出口处收集一试管气体,验纯;
e.点燃A处倒扣漏斗尖嘴。
正确的实验操作顺序是__________________________。
(3)E装置中澄清石灰水的作用是__________________;
F装置中澄清石灰水的作用是______________________;
(4)查阅相关资料发现:乙二酸又名草酸,是二元弱酸,易溶于水,酸性比碳酸强,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色难溶物。进一步研究会对甲同学实验中CO2的检验.提出质疑。试指出原设计中存在的问题,并提出实验的改进措施:________
_____________________________________________________________________________________________________________________________________________________________。
Ⅱ.乙同学利用乙二酸的还原性来测定草酸亚铁(FeC2O4)样品的纯度。已知:
2MnO4-+5C2O42-+F16H+==10CO2↑+2Mn2++8H2O
MnO4-+Fe2++t+H+-Mn2++Fe3++H2O(未配平)
现称取草酸亚铁(FeC2O4)样品2.88g(其中的杂质不与酸性高锰酸钾溶液反应),再将其溶于稀硫酸,然后用0.300 mol·L-1的酸性高锰酸钾溶液滴定,当消耗了36.0 mL酸性高锰酸钾溶液时,溶液立即由无色变为紫红色,且30s内不褪色即达到滴定终点。
(1)试配平下列离子方程式。
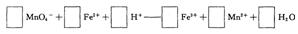
(2)求样品中草酸亚铁的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com