
28.(6分)将4g NaOH固体溶于水配成250mL溶液,取出10mL.此溶液,然后加水稀释到
100mL。求:
(1)取出的10mL NaOH溶液中含NaOH的质量;
(2)稀释后溶液中NaOH的物质的量浓度。
27.(6分)
(1)含0.4mol A13+的Al2(SO4)3中所含的SO42-的物质的量是_____________;
(2)已知16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
________________________________________________;
(3)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为
阿伏加德罗常数)____________________。
26.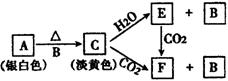 (7分)现有A、B、C、E、F五种物质,A、B是两种常见的单质,C、E、F是三种常见的化合物,它们之间的相互转化关系如图示。
(7分)现有A、B、C、E、F五种物质,A、B是两种常见的单质,C、E、F是三种常见的化合物,它们之间的相互转化关系如图示。
(1)写出A、B、C、E、F的化学式:
A__________、B________、C_________、
E__________、F________;
(2)写出E转化为F的离子方程式:____________。
25.(9分)实验室配制500mL0.5mol·L-1的NaOH溶液,有如下操作步骤:
①把称好的NaOH放入小烧杯中。加入适量的蒸馏水溶解、冷却;
②把①所得溶液小心转入500mL容量瓶中;
③继续向容鳍瓶中加蒸馏水至液面距刻度线l-2cm处,改用胶头滴管小心加蒸馏水至溶液凹液面底部与刻度线相切;
④用少量蒸馏水洗涤烧杯2-3次,每次洗涤的液体都小心用同一玻璃棒引流转入容最瓶并轻轻摇匀;
⑤将容量瓶塞紧瓶塞,充分摇匀。
回答下列问题:
(1)要配制氢氧化钠溶液,在用托盘天平称量氢氧化钠固体时,托盘天平的读数是________
(填代号,下同);
A.10.0g B.10.00g C.>10.0g D.<10.0g
 (2)本实验操作步骤的正确顺序是(填序号)_____________________;
(2)本实验操作步骤的正确顺序是(填序号)_____________________;
(3)本实验用到的基本仪器除了天平、药匙、玻璃棒、烧杯以外,
还需要的仪器有_________________;
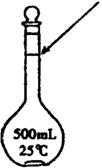
(4)某同学观察液面的情况如图所示,对所配溶液的物
质的量浓度有何影响? ____________________(填“偏高”、“偏
低”或“无影响”);
(5)在配制溶液的过程中,下列操作能造成结果偏
低的是________________。
A.容量瓶不干燥,含有少量蒸馏水 B.溶解所用烧杯未洗涤
C.NaOH溶解后,未冷却即进行实验 D.定容后摇匀,发现液面低于刻度线
24.(4分)某城市居民用现放出来的自来水直接养鱼,结果造成鱼死亡。
试解释其原因:_______________________________________________________;
正确的做法是:______________________________________________________。
23.(4分)一个体重50kg的健康人含铁元素2g。这2g铁以Fe2+和Fe3+的形式存在。Fe2+易被吸收,给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4).服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)人体中经常进行Fe2+ 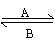
 Fe3+的转化,在过程A中,Fe2+被___________,过程B中,Fe2+是___________产物;
Fe3+的转化,在过程A中,Fe2+被___________,过程B中,Fe2+是___________产物;
(2)“服用维生索C可使食物中的Fe3+转化为Fe2+”这句话指出,维生素C在这一反应过程中做_________剂,具有_________性。
22.(8分)在编号为A、B、C、D的四支试管中分别盛有NaHSO4、NaHCO3、BaCl2、BaCO3固体,在只有蒸馏水和若干试管的条件下,将它们一一鉴别出来,在你设计的实验方案中:
(1)已知NaHSO4溶于水发生电离:NaHSO4=Na++H++SO42-,根据物质的溶解性不同,最先检验出来的固体是_______,随后枪验出的第二种物质是_______;
(2)后两种固体被检验出来时发生反应的离子方程式分别是
____________________________________、____________________________________。
21.(6分)下表是某地市场销售的一种“加碘食盐”包装袋上的部分文字说明。
|
配料 |
氯化钠、碘酸钾(KIO3) |
|
含碘量 |
20-40mg·kg-1 |
|
保质期 |
18个月 |
|
食用方法 |
勿长时间炖炒 |
|
贮藏指南 |
避热、避光、密封、防潮 |
(1)碘酸钾属于__________(填“氧化物”、“酸”或“盐”),其中碘元素的化合价为__________;
(2)根据“加碘食盐”的食用方法,可推测碘酸钾在受热时__________________。
20.VL Mg(NO3)2溶液跟VL NaNO3溶液混合后,NO3-的物质的量浓度为1.5mol·L-1,则原Mg(NO3)2和NaNO3溶液的物质的最浓度(设混合液的体积等于两溶液的体积之和)可能是
A.都是1.5mol·L-1 B.都是1mol·L-1
C.2mol·L-1和0.5mol·L-1 D.0.5mol·L-1和2mol·L-1
第Ⅱ卷 (非选择题 共50分)
19.下列有关实验操作不正确的是

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com