
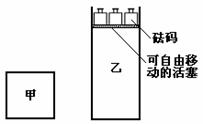
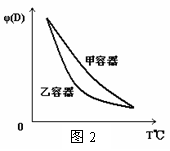
11.一定温度下,有可逆反应:2A(g)+2B(g) C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
|
关于两容器中反应的说法正确的是
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2 所示
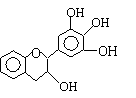 D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍 12.“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍 12.“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是
A、分子中所有的原子共面
B、1molEGC与4molNaOH恰好完全反应
C、易发生氧化反应和取代反应,难发生加成反应
D、遇FeCl3溶液不发生显色反应
10.在由水电离产生的c(H+)=10-12mol·L-1的溶液中,一定不能大量共存的离子组是
A.NH4+、Ba2+、Cl-、NO3- B.Cl-、SO42-、Na+、K+
C.SO42-、NO3-、Fe2+、Mg2+ D.Na+、K+、ClO-、S2-
9.设NA为阿伏加德罗常数,下列说法正确的是
A.58.5g氯化钠中约含有6.02×1023个氯化钠分子
B.含有2NA个阴离子的CaC2,在标准状况下,能产生约44.8L的乙炔气体
C.在含4mol Si-O键的石英晶体中,氧原子的数目为4NA
D.12.5 mL 16 mol·L-1浓硫酸与足量锌反应,转移电子数为0.2NA阿伏加德罗常数
约为6.02×1023 mol-1,
8.下列说法或表示方法正确的是
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(石墨)→C(金刚石);ΔH= +119 kJ/mol可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);ΔH= -57.3 kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1 mol NaOH的稀溶液混合,放出的热量大于57.3 kJ
D.在101kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);ΔH= -285.8 kJ/mol
7.甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,下列判断正确的是
A.甲由水电离出来的H+的物质的量浓度是乙的 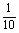 倍
倍
B.物质的量浓度c(甲)=10c(乙)
C.中和等物质的量的NaOH溶液需甲、乙两杯酸的体积,10V(甲)>V(乙)
D.甲中的c(OH-)为乙中c(OH-)的10倍
6.甲、乙都是短周期元素,其中甲元素原子的最外层电子数是次外层电子数的2倍,乙元素原子K层和M层电子数之和与L层的电子数相同。下列判断不正确的是
A.乙元素的族序数比甲元素的族序数大
B.乙元素最高价含氧酸酸性比甲元素最高价含氧酸酸性强 C.乙元素的原子序数比甲元素的原子序数大
D.含乙元素的化合物数目比含甲元素的化合物数目多
5.下列离子方程式表示正确的是
A.等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:
HCO3-+Ba2++OH-=BaCO3↓+H2O
B.向小苏打溶液中加入醋酸溶液:HCO3-+H+=CO2↑+H2O
C.氯化铁溶液中加入铜片:Fe3++Cu=Fe2++Cu2+
D.NaHCO3的水解:HCO3-+H2O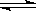 H3O++CO32-
H3O++CO32-
4.下列顺序排列中正确的是
A.沸点:HI>HBr>HCl>HF B.熔点:PF3>PCl3>PBr3>PI3
C.化合物数目种类;C>H>Si>S D.酸性:HClO4>HNO3>H3BO3>H2CO3
3.下列说法正确的是:
A.HI的相对分子质量大于HF,所以HI的沸点高于HF
B.由ⅠA和ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子型化合物
C.H与D、16O与18O 互为同位素,H2、D2互为同素异形体
D.在SiO2 晶体中,1个Si原子和2个O原子形成2个共价键
2.分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
① 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
② 根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③ 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④ 根据反应中的热效应将化学反应分为放热反应和吸热反应
A.①③ B.②④ C.①②④ D.②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com