
20.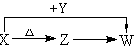 (12分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。请回答:
(12分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。请回答:
(1)W的电子式是___________。
(2)X与Y在溶液中反应的离子方程式是___________________________________。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
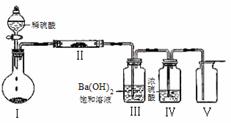
①装置Ⅰ中反应的化学方程式是___________________,
装置Ⅱ中物质的化学式是_____________________________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是____________,所需仪器装置是_____________(从上图中选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是___________________________ 。
19.(14分)A、B、D、E是周期表中前20号元素,它们的原子序数依次增大。EA2与水反应产生可燃性气体和白色浆状物,向该浆状物中通入AB2气体可得另一白色不溶物。B、D同主族,D的阴离子与E的阳离子具有相同的核外电子排布。请回答:
(1)写出元素符号:A_________、B_________。
(2)已知AD2与AB2的结构相似,AD2的结构式为___________,该分子是___________(填“极性分子”或“非极性分子”)。
(3)镁条在AB2中燃烧的化学方程式为_________________________________。
(4)将D单质放入浓HNO3中加热,生成红棕色气体和一种强酸,该反应的离子方程式为______________。
(5)A可形成二元弱酸H2A2O4。0.1 mol H2A2O4与100 mL 2 mol·L-1的KOH溶液反应后,溶液中的离子浓度由大到小的排列顺序是__________________。
18.(12分)科学家从化肥厂生产的(NH4)2SO4中检验出组成为N4H2(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N4H24+两种形式存在,植物的根系极易吸收N4H24+,但它遇到碱时,会生成一种形似白磷的N4分子,N4不能被植物吸收。请回答下列问题:
(1)N4和N2的关系正确的是_______(填序号)
A.同种单质 B.同位素 C.同分异构体 D.同素异形体
(2)N2H4(SO4)2______(填“能”或“不能”)与草木灰混合使用。
(3)已知白磷、NH4+、N4H44+的空间构形均为四面体,NH4+的结构为: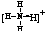 (→表示共用电子对有N原子单方面提供),白磷(P4)的结构为
(→表示共用电子对有N原子单方面提供),白磷(P4)的结构为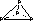 。请画出N4H4+的结构式:_____________________。
。请画出N4H4+的结构式:_____________________。
(4)已知液氨中存在着平衡:2NH3 NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式____________________。
NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式____________________。
(5)含有一定量(NH4)2SO4和NH3·H2O的水溶液称为“缓冲溶液”在此溶液中加入少量的强酸或者强碱时,溶液的pH几乎不变,这可由下列离子方程式来说明。
加酸时:NH3·H2O+H+=NH4++H2O 加碱时:NH4++OH-=NH3·H2O
由于(NH4)2SO4和NH3·H2O的大量存在,加少量酸或碱时,溶液中c(H+)与c(OH-)基本保持不变;含有一定量NaH2PO4和Na2HPO4的溶液,也具有缓冲作用,写出此溶液中加入少量强酸或者强碱时发生的离子反应方程式:加酸时:_____________;加碱时:__________。
17.对于反应:As2S3+3S22-=2AsS43-+S的正确说法是
A.属于置换反应 B.S22-只是还原剂
C.As2S3是还原剂 D.AsS43-既是氧化产物又是还原产物
16.关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加入AgNO3溶液,生成白色沉淀,加盐酸沉淀不消失,则原溶液中有C1-存在
B.加入Ba(NO3)2溶液,生成白色沉淀,加盐酸沉淀不消失,则原溶液中有SO42-存在
C.先通入C12,溶液变黄棕色;再滴入淀粉试液后,溶液又变蓝,则原溶液中有I-存在
D.加入盐酸,生成了能使澄清石灰水变浑浊的气体,则原溶液中有CO32-存在
15.下列事实能用同一原理解释的是 A.SO2和Cl2都能用于漂白 B.苯酚、乙烯都能跟溴水反应
C.苏打、小苏打水溶液的pH都大于7 D.I2、NH4Cl晶体受热都逐渐消失
14.固体A的化学式为NH5,能跟水反应,它的所有原子的电子层结构都跟该原子同周期的稀有气体原子一样,则下列说法中,不正确的是
A.1 mol NH5中有5NA个N-H键(NA为阿伏加德罗常数)
B.NH5中既有共价键,又有离子键,是离子晶体
C.NH5跟水的反应是氧化还原反应
D.NH5跟水反应的化学方程式为:NH5+H2O=NH3·H2O+H2↑
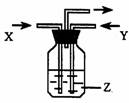
13.下列各组物质中,气体X和气体Y同时通入盛有溶液Z的洗气瓶中(下图所示),一定没有沉淀生成的是
|
|
X |
Y |
 Z Z |
|
A |
NO2 |
SO2 |
BaCl2 |
|
B |
NH3 |
O2 |
Al2(SO4)3 |
|
C |
NH3 |
CO2 |
CaCl2 |
|
D |
CO2 |
SO2 |
CaCl2 |
12.下列离子方程式正确的是
A.等体积等物质的量浓度的醋酸与纯碱两溶液相混合:2CH3COOH+2H+=CH3COO-+CO2↑+2H2O
B.Fe(NO3)2溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
C.将等物质的量的C12和SO2与水充分反应:C12+SO2+2H2O=4H++SO42-+2Cl-
D.A1C13溶液和过量的氨水反应:Al3++4OH-=AlO2-+2H2O
11.青石棉(cricidolite)是世界卫生组织确认的一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,青石棉的化学式为:Na2Fe5Si8O22(OH)2,青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法正确的是
A.青石棉是一种易燃品且易溶于水
B.青石棉的化学组成用氧化物的形式可表示为:Na2O·3FeO ·Fe2O3·8SiO2 ·H2O
C.1 mol Na2Fe5Si8O22(OH)2与足量的硝酸作用,至少需消耗6 L 3 mol·L-1HNO3溶液
D.1 mol Na2Fe5Si8O22(OH)2与足量氢氟酸作用,至少需消耗5.5 L 2 mol·L-1HF溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com