
12.下列说法中不正确的是:
A.增大反应物浓度,可使单位体积内活化分子数增加,反应速率加快
B.在其它条件不变时,升高温度一定会加快化学反应的反应速率
C.使用合理的催化剂,可以改变化学反应速率,但不能改变化学平衡状态
D.对于任何化学反应来说,反应速率越大,反应现象就越明显
11.下列各组离子能大量共存,当溶液中C(H+)=10-1mol·L-1时,有气体产生;而当溶液中C(H+)=10-13mol·L-1时,又能生成沉淀。则该组离子可能是:
A.Na+、Cu2+、NO3-、CO32- B.Ba2+、K+、Cl-、HCO3-
C.Fe2+、Na+、SO42-、NO3- D.Mg2+、NH4+、SO42-、Cl-
10.下列各组物质的颜色变化,可用勒夏特列原理解释的是:
A.光照氯水,颜色变浅
B.向盛有NO2的集气瓶中投入活性炭,颜色变浅
C.加热氯化铁溶液,溶液变浑
D.压缩H2与I2(g)反应的平衡混合气体,颜色变深
9、设NA表示阿伏加德罗常数,下列有关说法正确的是( )
A.当活泼金属转移2NA个电子时,可从盐酸中置换出22.4LH2
B.53.5gNH4Cl中含有H-Cl键的个数为4NA
C.用惰性电极电解500mL饱和食盐水时,若溶液的pH变为13时,则电极上转化的电子数目约为3.01×1022(忽略溶液的体积变化)
D.在标准状况下,2.24L的己烷中含有共价键的数目约为1.9×6.02×1023
8.已知乙烯和乙炔燃烧的热化学方程式分别为:
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH= -2600 kJ·mol―1
C2H4(g)+3O2(g)=2CO2(g)+2H2O(l);ΔH= -1411 kJ·mol―1
又知氧炔焰的温度比乙烯燃烧时火焰的温度高。据此,下列说法错误的是
A.物质的燃烧热越大,火焰温度越高
B.烃完全燃烧时,火焰温度的高低不仅仅取决于其燃烧热的高低
C.相同条件下等体积乙烯和乙炔完全燃烧时,乙炔放热较少
D.1mol乙烯完全燃烧生成气态产物时,放出的热量小于1411 kJ
7.工业上由二氧化锰制备高锰酸钾可分二步进行,第一步二氧化锰与氢氧化钾共熔并通入氧气: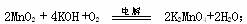 第二步:电解锰酸钾溶液:
第二步:电解锰酸钾溶液:
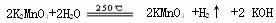 下列说法叙述正确的是( )
下列说法叙述正确的是( )
A.该条件下氧化性:KMnO4 >K2MnO4 >O2
B.根据上述过程,每生成1molKMnO4共转移6mol电子
C.第二步电解时,KMnO4在阳极区生成
D.第二步电解时阴极周围pH减小
6.室温下对pH相同、体积相同的醋酸和硫酸两种溶液分别采取下列措施,有关叙述中正确
的是
A.加水稀释2倍后,两溶液的pH均减小
B.使温度都升高20℃后,两溶液的pH均不变
C.加适量的醋酸钠晶体后,两溶液的pH均增大
D.加足量的锌充分反应后,两溶液中产生的氢气一样多
5.下列实验中,仪器的下端必须插入液面下的是 ( )
①制备氢气的简易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗;
③制备Fe(OH)2操作中的胶头滴管; ④制乙酸乙酯时插入碳酸钠溶液中的导管
⑤用乙醇制取乙烯时的温度计; ⑥分馏石油时的温度计
A ①③⑤ B ②④⑥ C ①③④⑤ D 全部
4.下列金属组合中,一般用电解法冶炼的是
A.Fe、Hg、Na B.A1、Na、K C.A1、Fe、Ag D.Cu、Ag、Au
3.要使氯化铝溶液中的A13+完全转化成A1(OH)3沉淀,应选用的试剂是:
A.NaOH溶液 B.稀盐酸 C. 氨水 D.AgNO3溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com