
3、下列说法中正确的是( )
A,Na在空气中缓慢氧化生成白色的Na2O2 B,Na在空气中燃烧生成Na2O2
C,Na在空气中燃烧生成淡黄色的Na2O D,Na在空气中燃烧生成白色的Na2O2
2、下列关于钠的单质的说叙述中,正确的为( )
A,化学性质比较活泼,所以自然界中无游离态的钠
B,不能保存在水中是因为钠的密度比水小
C,是一种较硬的金属,导热性好
D,熔沸点较高
1、下列为强电解质的是( )
A,H2SO4 B,Fe C,CH3COOH D,酒精
18.(11分)将1 mol I2(g)和2 mol H2置于某2 L密闭容器中,在一定温度下发生反应:I2(g)+H2 (g)  2HI
(g);△H>0,并达平衡.HI的体积分数φ (HI)随时间变化如图曲线(b)所示:
2HI
(g);△H>0,并达平衡.HI的体积分数φ (HI)随时间变化如图曲线(b)所示:
 (1)达平衡时,I2 (g)的物质的量浓度为____________。
(1)达平衡时,I2 (g)的物质的量浓度为____________。
(2)若在相同条件下,向容器内加入1 mol H2和2 mol HI,达平衡时HI的转化率为____________。
(3)若改变反应条件,在甲条件下,φ (HI)的变化如图曲线(a)所示,在乙条件下,φ (HI)的变化如图曲线(c)所示.则甲条件可能是___________(填入下列条件的序号,下同),乙条件可能是__________。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温恒容条件下,加入适当催化剂
(4)若保持温度不变,在另一相同的2 L密闭容器中加入x mol I2(g)、y mol H2和z mol HI(x、y、z均大于0),发生反应,达平衡时,HI的体积分数仍为0.60且其它成分体积分数与上述平衡相同,则x、y、z的关系是_________________。
17.(15分)A、B、C、D是化学中常见的单质,其中A是用量最大、应用最广泛的金属,D是地壳中含量最多的金属元素,甲、乙、丙为化合物,其中甲为黑色晶体,乙在常温常压下为无色无味的液体.它们之间存在如图所示的转化关系,由此可推知:

(1)元素D在周期表中的位置为___________。
(2)写出甲和D反应的化学方程式(注明条件)____________________________,在此反应中生成1 mol A转移电子的物质的量为__________mol。
(3)已知D能与烧碱溶液反应,写出D与烧碱溶掖反应的离子方程式:_______________
___________________________________________。
(4)元素A的高价氯化物常用于净水,请用离子方程式表示其净化原理_______________
___________________________________________。
(5)有一块A与D的合金,溶于足量盐酸中,再用过量的NaOH溶液处理,将产生的沉淀过滤、洗涤、干燥并灼烧后,完全变为红色粉末.称量,发现此红色粉末与原合金质量恰好相等.则合金中铝的质量分数为___________。
16.(14分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大.A元素的原子是半径最小的原子.B元素的最高价氧化物对应水化物与其氢化物反应生成一种盐X.D与A同主族,且与E同周期.E元素的最外层电子数是其次外层电子数的3/4倍,A、B、D、E这四种元素,每一种与C元素都能形成元素的原于个数比不同的若干种化合物.请回答下列问题:
(1)①写出元素的元素符号:B___________,C__________
②写出A与B形成化合物电子式_______________,其分子构型为______________。
(2)E的最高价态与A、B、C三种元素形成酸式盐Y的化学式是_________,该盐在水溶液中的离子浓度由大到小的顺序是_____________________________。
(3)常温时,B元素的最高价氧化物对应水化物Z的溶液与盐X的溶液的pH均为a,这两种溶液中由水电离出来的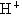 浓度分别用c(
浓度分别用c(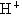 )1、c(
)1、c(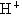 )2表示,则c(
)2表示,则c(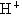 )1∶c(
)1∶c(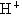 )2=___________。
)2=___________。
15.(18分)某学生设计了一套验证物质化学性质的实验装置(如下图),请完成下列问题:

(1)该实验的目的是:_________________________________________________________
_______________________________________________________________。
(2)该实验的原理是(用化学方程式表示)________________________________________、
__________________________________________。
(3)实验用品:实验仪器除铁架台(带铁夹)、储气瓶(两个),直管活塞(K1、K2)、止水夹(K3)、橡胶管、橡胶塞以及若干玻璃管连件外,还有哪几种(写仪器名称)__________,实验所用试剂为____________________________。
(4)检查本装置气密性的最好方法是:___________________________________________
_______________________________________________________________________________
______________________________________________________________________。
(5)实验步骤:①按上图连接好仪器装置,②扭开活塞K1和K2,主要现象为:________
_____________________________________。③关闭活塞K1和K2,打开止水夹K3,要使烧瓶内产生喷泉可采用的方法是:___________________________________________________
___________________________________________________________。
14.将5.4g Al投入到200.0 mL 2.0 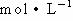 的某溶液,生成的气体只有氢气,充分反应后有金属剩余.该溶液可能为
的某溶液,生成的气体只有氢气,充分反应后有金属剩余.该溶液可能为
A.HNO3溶液 B.Ba(OH)2溶液 C.H2SO4溶液 D.HCl溶液
第Ⅱ卷(非选择题,共58分)
13.将Na2CO3·10H2O和NaHCO3的混合物n g,溶于水制成200 mL溶液,c( )=0.5 mol/L若将n g该混合物加热至质量不再改变时,剩余固体的质量可能是
)=0.5 mol/L若将n g该混合物加热至质量不再改变时,剩余固体的质量可能是
A.3.1 g B.5.3 g C.9.0 g D.11.0 g
12.下列实验操作正确的是
A.试管内装有1/5的溶液,则溶液的体积约为2 mL
B.拟在加热条件下配制40 mL溶液,应选择的烧杯规格是50 mL
C.腐蚀性的药品应放在烧杯中称量,其它固体药品可直接放在托盘上
D.实验室配制一定浓度的稀硫酸,应将浓硫酸沿烧杯壁慢慢倒入水中,并不断搅拌
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com