
8.下列说法中正确的是[ ]
A. ⅠA、ⅡA族元素的原子,其半径越大,越难失去电子
B. 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
C. 原子及其离子的核外电子层数等于该元素所在的周期数
D. 所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等
7.肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气。已知:N2(g) + 2O2(g)=N2O4(g); △H=+ 8.7kJ/mol
N2H4(g) + O2(g)=N2(g) + 2H2O(g); △H=–534 kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是[ ]
A. 2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g); △H=–1076.7 kJ/mol
B.
N2H4(g) + 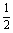 N2O4(g) =
N2O4(g) =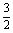 N2(g) + 2H2O(g); △H=–1076.7 kJ/mol
N2(g) + 2H2O(g); △H=–1076.7 kJ/mol
C. 2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g); △H=–542.7 kJ/mol
D. 2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g); △H=–1059.3 kJ/mol
6.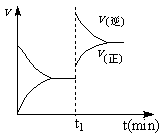 下图为某化学反应速率-时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是
下图为某化学反应速率-时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是
A.2SO2 (g)+O2 (g) 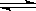 2SO3
(g) ;△H<0
2SO3
(g) ;△H<0
B.4NH3 (g)+O2 (g) 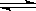 4NO(g)+6H2O (g) ;△H<0
4NO(g)+6H2O (g) ;△H<0
C.H2 (g)+I2 (g)
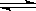 2HI
(g) ;△H>0
2HI
(g) ;△H>0
D.C (s)+H2O (g) 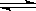 CO (g)+H2 (g) ;△H>0
CO (g)+H2 (g) ;△H>0
5.食品中含有过量的 (丙烯酰胺)可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述:①能使酸性高锰酸钾溶液褪色,②能发生加聚反应,③能与氢气发生加成反应, ④是高分子化合物。其中正确的是[ ]
A.①②④ B.②③④ C.①②③ D.①③④
4.金属钛对体液无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关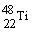 和
和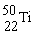 的说法中正确的是[ ]
的说法中正确的是[ ]
A.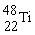 和
和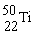 原子中均含有22个中子
原子中均含有22个中子
B.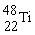 和
和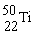 在周期表中位置相同,都在第4纵行
在周期表中位置相同,都在第4纵行
C.分别由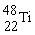 和
和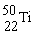 组成的金属钛单质互称为同分异构体
组成的金属钛单质互称为同分异构体
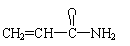 D.
D.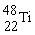 与
与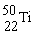 为同一核素
为同一核素
3.巴豆酸的结构简式为CH3CH=CHCOOH ,现有
①水 ②溴的四氯化碳溶液 ③丁醇 ④纯碱溶液 ⑤酸性KMnO4溶液。
在一定条件下,能与巴豆酸反应的物质组合是[ ]
A.只有②④⑤ B.只有②③⑤ C.只有②③④⑤ D.①②③④⑤
2.NA为阿伏加德罗常数,下列说法中正确的是[ ]
A.用稀氢氧化钠溶液吸收氯气22.4L,反应中转移的电子数目为NA
B. 1mol/L Mg(NO3)2溶液中含有NO3-的数目为2NA
C. 室温下,28.0g乙烯和丙烯混合气体中含有的碳原子数为2NA
D. 标准状况下11.2L臭氧中含有的氧原子数目为3NA
1.下列叙述不正确的是[ ]
A.金刚砂的成分是Al2O3,可用作砂纸、砂轮的磨料
B.水晶和玛瑙的主要成分都是SiO2
C.含硅的钢具有良好的导磁性
D.太阳能电池可用硅材料制作,其应用有利于环保、节能
25、(8分)某资料说铁锈的成分为Fe2O3·H2O和FeCO3的混合物。根据此记载,某实验兴趣小组设计下列实验来验证其中是否含有碳酸亚铁。
①取一高度腐蚀的干燥铁钉,称其质量为10.04g,在氮气保护下,充分加热,冷却后称得质量为8.92g。
②将①得到的残渣投入到5.00mol/L的硫酸中,不断添加硫酸直至残渣完全溶解时,恰好用去硫酸31.00mL。整个过程无气体放出。试回答下列问题:
⑴铁锈中是否含有碳酸亚铁?理由是?
⑵锈蚀的铁钉中含Fe2O3·H2O多少克? ⑶锈蚀前铁钉的质量至少多少克?
24、(6分)将3.20g Cu溶于B mol/L过量的硝酸溶液30.0 mL中,假设硝酸的还原产物只有NO2和NO,反应结束后,将所剩溶液加水稀释至1000 mL,测得c(NO3-)=0.200 mol/L。
(1)试求稀释后溶液的pH。
(2)生成的气体中NO2和NO的物质的量(可以含有B的代数式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com