
11.有五个系列同族元素的物质,101.3kP时测定它们的沸点(℃)如下表所示:
|
① |
He -268.8 |
(a) -249.5 |
Ar -185.8 |
Kr 151.7 |
|
② |
F2 -187.0 |
Cl2 -33.6 |
(b) 58.7 |
I2 184.0 |
|
③ |
(c) 19.4 |
HCl -84.0 |
HBr -67.0 |
HI -35.3 |
|
④ |
H2O 100.0 |
H2S -60.0 |
(d) -42.0 |
H2Te -1.8 |
|
⑤ |
CH4 -161.0 |
SiH4 -112.0 |
GeH4 -90.0 |
(e) -52.0 |
对应表中内容,下列叙述中正确的是
A.a、 b、c的化学式分别为Ne、Br2、HF
B. 系列②物质均有氧化性;系列③物质对应水溶液均是强酸
C.系列④中各化合物的稳定性顺序为:H20>H2S>H2Se>H2Te
D.上表内物质HF和H2O,由于氢键的影响,其分子特别稳定
10.下列离子方程式正确的是
A.硫酸铝溶液中加过量氨水:Al3+ + 4OH- = AlO2- + 2H2O
B.向硅酸钠溶液中通入过量的CO2: SiO32- + 2CO2 + 2H2O = H2SiO3↓+ 2HCO3-
C.过量铁粉与一定量稀硝酸反应:Fe+4H++NO3-=Fe3++NO↑+2H2O
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全:
Ba2+ + 2OH- + NH4+ +H+ + SO42- = BaSO4↓+ NH3·H2O + H2O
9.阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是
A.标准状况下,1.12L的SO3所含的原子数约为0.2×6.02×1023
B.在标准状况下,2.24L一氧化氮与氮气混合气所含分子数约为0.1×6.02×1023
C.1molCH3+(碳正离子)中含电子数目约为10×6.02×1023
D.1molD2O含有的中子数约为8×6.02×1023
8.将0.1 L含有0.02mol CuSO4和0.01molNaCl的水溶液用惰性电极电解。电解一段时间后,一个电极上得到0.01 mol Cu,另一电极析出的气体
A.只有Cl2 B.只有O2 C.既有Cl2又有O2 D.只有H2
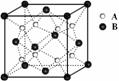
7、某离子晶体的晶体结构中最小重复单元如图所示:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为
A、B2A B、BA2 C、B7A4 D、B4A7
6.对下列各种溶液中所含离子的判断合理的是
A. 向无色溶液中加氯水变橙色,溶液中可能含: SO42-,Br-,OH-,Ba2+
B.在c(H+)=10-14mol/L的溶液中可能含:Na+,A102-,CO32-,SO32-
 C.
某溶液,加铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3-
C.
某溶液,加铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3-
D.使紫色石蕊试液变红色的溶液中可能含:K+,Na+,Ca2+,HC03-
5.肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气。已知:
N2(g)+2O2(g)=N2O4(g);△H=+8.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.0kJ/mol
下列表示肼跟N2O4反应的热化学方程式,正确的是
A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-542.7kJ/mol
B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1059.3kJ/mol
C.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1076.7kJ/mol
D.N2H4(g)+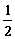 N2O4(g)=
N2O4(g)=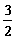 N2(g)+2H2O(g);△H=-1076.7kJ/mol
N2(g)+2H2O(g);△H=-1076.7kJ/mol
4.下列各组物质有关物理性质的比较中,前者大于后者的是
A.密度:氯丁烷与氯丙烷 B.硬度:晶体硅与金刚石
C.沸点:硬脂酸与软脂酸 D.水溶性:小苏打与苏打
3. 右图是制取和收集某气体的实验装置,该装置可用于
右图是制取和收集某气体的实验装置,该装置可用于
A.用浓盐酸和二氧化锰反应制取Cl2
B.用浓氨水和生石灰反应制取NH3
C.用浓硝酸与铜反应制取NO2
D.用过氧化钠固体和水反应制取O2
2.下列八种试剂中:①酚酞试液 ②银氨溶液 ③稀H2SO4 ④Na2SO3溶液 ⑤FeCl3溶液(加少量HCl) ⑥氢硫酸 ⑦Na2CO3溶液 ⑧石灰水 都不宜长期放置的组合是
A.②④⑥⑧ B.①②④⑥⑧ C.②③⑤⑦ D.②④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com