
5.保护环境,人人有责。下列说法错误的是 ( )
A.倡导人们在购物时使用纸袋或布袋、最好不用塑料袋,是为了防止白色污染
B.对废电池集中处理是为防止电池中汞、镉、铅等重金属离子对土壤和水源的污染
C.北京地区空气污染指数的主要项目是:SO2、NO2、CO2及可吸入颗粒物
D.白口铁(镀锌铁)和马口铁(镀锡铁)比较,镀层被破坏后,马口铁更易被腐蚀
28.(14分)铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸。某化学研究小组在实验室中按下列步骤模拟该生产过程。填写下列空白。

(1)配制溶液。需要配制200mL密度为1.2g·cm-3的溶质质量分数为16%的NaOH溶液,该NaOH溶液的物质的量浓度为_________mol/L;
(2)把铝片浸入热的16%NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗。写出除去氧化膜的离子方程式 _________ ;
(3)如图组装好仪器,接通开关K,通电约25min。在阳极生成氧化铝,阴极产生气体。写出该过程中的阴极电极反应式:______________ ;
(4)断开电路,取出铝片,用1%稀氨水中和表面的酸液,再用水冲洗干净,即完成。
(5)如果去掉装置图中的电源和滑动变阻器,用导线直接把除去氧化膜后的铝片与碳棒连接,则该装置中铝片端是_____极,电子流动的方向由____极到____极,每转移1.5mol电子,溶液质量增加_____g,假设一段时间后,硫酸全部消耗完,所得溶液中离子浓度由大到小的顺序为________。
27.(14分)中学化学中常见的几种物质存在如下关系,其中甲是黑色非金属单质,乙是生活中常见的金属单质,D是红棕色气体。(图中部分产物和反应条件已略去)
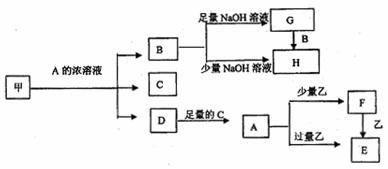
回答下列问题:
(1)写出甲与A的浓溶液反应的化学方程式_______________ ;
(2)C的电子式是 ________________;
(3)除去G固体中含有H杂质采用的方法是_______________;
(4)A溶液与一种能使湿润的红色石蕊试纸变蓝的气体反应,生成一种盐,该盐的溶液呈酸性,其原因是(用离子方程式表示)_____________________;
(5)写出由F转化为E的离子方程式____________ ;将溶液F加热蒸干、灼烧到质量不再减少时所得固体物质的化学式为_______________;
(6)4g单质甲燃烧能放出131.17kJ的热量,写出单质甲燃烧热的热化学方程式_______;
26.(16分)实验室可采用下列装置制取纯净的氯气(可含水蒸气),并用氯气和Ca(OH)2反应制取少量漂白粉。已知氯气和Ca(OH)2制取漂白粉的反应是放热反应,温度稍高即发生副反应。
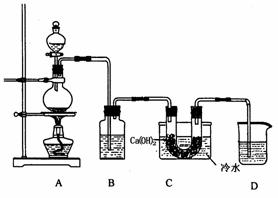
(1)B中盛放的试剂是______________________;
D装置的作用是 ______________________ ;
(2)写出实验室制取氯气的离子方程式__________________;
(3)已知氯气和Ca(OH)2温度稍高发生副反应,生成两种含氯元素的盐和水,每0.3mol氯气参加反应,转移电子0.5mol,写出该副反应发生的化学方程式________;
(4)若将装置D改为收集装置,也可以采用以上装置中的一些仪器,在实验室制备其它纯净、干燥的气体。在下表中填入最合适的试剂(如有需要,装置A中的加热仪器和C中的冷水可以撤去,可添加温度计,装置B可重复使用)。
|
要制取的气体 |
A装置中药品 |
除杂装置B中的试剂 |
干燥装置B或C中的试剂 |
|
CO2 |
石灰石、稀盐酸 |
_____________ |
________________ |
|
C2H4 |
____________ |
_____________ |
碱石灰 |
25.(16分)有机化合物A(C5H8O2)不溶于水,并可以发生如下图所示的变化:
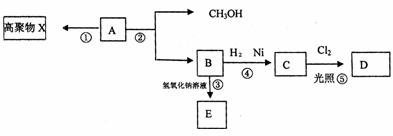
已知:C的一氯代物D只有两种
请回答:
(1)A分子中含有的官能团的名称_________;
(2)①②④⑤反应中属于取代反应的有___________(填序号);
(3)C的结构简式 __________,
X结构简式 _____________;
(4)写出②的反应方程式 ____________________________________;
(5)C的同分异体中属于酯类的有_______种,写出其中的结构简式_______,__________.
(6)简述检验D中含有氯元素的方法___________________ ;
(7)17.2gB与足量的碳酸氢钠溶液反应,标准状况下生成二氧化碳的体积为________L。
12.25℃时有三瓶溶液:pH=3的盐酸、pH=3的醋酸溶液和pH=11的氢氧化钠溶液,下列说法正确的是 ( )
A.中和等体积pH=11的氢氧化钠溶液,所需pH=3醋酸溶液的体积大于pH=3盐酸的 体积
B.在等体积pH=3盐酸和pH=3醋酸溶液中分别加入少量相同的锌粒,盐酸中的锌粒 先反应完
C.当pH=3的醋酸溶液和pH=11的氢氧化钠溶液混合得到pH=7的溶液时,该溶液中 c(Na+)大于c(CH3COO-)
D.25℃时pH=3的盐酸、pH=3的醋酸溶液中水电离出的c(H+)均为10-11mol/L
第II卷(非选择题 共180分)
本卷共11小题,共180分。
11.X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是 ( )
A.Y、Z两元素形成的简单阴离子的还原性Z>Y
|
C.X与W形成的化合物W2X2中含有离子键和共价键
D.Y、Z两种元素最高价氧化物对应水化物的酸性Z>Y
10. 在一密闭容器中,进行mX(g)+nY(s) 3Z(g);△H<0的反应,下列说法正确的是
在一密闭容器中,进行mX(g)+nY(s) 3Z(g);△H<0的反应,下列说法正确的是
( )
A.加入催化剂可以提高X的转化率
B.缩小容器的体积,混合体系中X的含量增加,则m一定小于3
C.降低温度,正反应速率增大,逆反应速率减小,混合体系中Z的含量增大
D.加入一些Y,平衡向右移动,可以提高X的转化率
9.下列各项中的两个量,其比值一定为2:1的是 ( )A.在反应2H2S+SO2=3S↓+2H2O中还原产物与氧化产物的质量
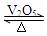 B.100mL 1mol/L Na2CO3溶液中c(Na+)与c(CO
B.100mL 1mol/L Na2CO3溶液中c(Na+)与c(CO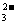 )
)
C.在密闭容器中,2SO2+O2 2SO3达到平衡量c(SO2)与c(O2)
D.Ba(OH)2溶液与明矾溶液完全反应,当铝元素全部以AlO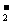 形成存在时,参加反应
形成存在时,参加反应
的Ba(OH)2与明矾的物质的量
8.下列五种有色溶液与SO2作用,均能褪色,其实质相同的是 ( )
①品红溶液 ②酸性KMnO4溶液 ③滴有酚酞的NaOH溶液 ④溴水 ⑤淀粉碘溶液
A.①④ B.①②④ C.②③⑤ D.②④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com