
12.在某无色溶液中,可能存在Na+、Ca2+、Fe3+、Br-、CO32-、SO42-、Cl-离子中的几种。某学生进行了下列实验:(1)取少量原溶液,在其中滴加足量氯水,有无色无味气体产生,溶液仍为无色,将溶液分为2份;(2)一份加入AgNO3溶液,有白色沉淀产生;(3)另一份加入BaCl2溶液,有白色沉淀产生。该溶液中一定大量存在的离子组是 ( )
A.Na+、Fe3+、SO42- B.CO32-、Cl-、SO42-
C.Ca2+、Br-、SO42- D.Na+、SO42-、CO32-
11.在120℃、101kPa下,amL由氢气、乙烯组成的混合气体在bmL氧气中充分燃烧后,恢复到原温度和压强。已知b > 3a,且燃烧后气体体积缩小了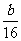 mL,则乙烯的体积为
mL,则乙烯的体积为
( )
A.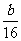 mL B.
mL B.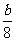 mL C.
mL C.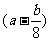 mL D.
mL D.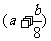 mL
mL
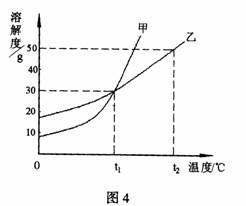
10.甲、乙两物体的溶解度曲线如图4所示。
|
A.t1℃时,在100g水中放入60g甲,其
溶质的质量分数为37.5%
B.t1℃时,甲和乙的饱和溶液的物质的量
浓度一定相等
C.t2℃时,甲和乙的饱和溶液中溶质的质
量数一定相等
D.t2℃时,分别在100g水中各溶解20g甲、
乙,同时降低温度,甲先达到饱和
9.下列实验操作正确的是 ( )
A.向过量稀硫酸中加入除去油污的废铁屑,是制备硫酸亚铁的可行方案
B.向碳酸钠粉末中加入乙二酸溶液,生成大量气泡,说明乙二酸的酸性比碳酸强
C.向铝屑与硫酸反应后的溶液中加入氧氧化钠溶液,是制备氢氧化铝的最佳方案
 D.向硫酸亚铁铵溶液中,依次加入氯水和硫氰化钾溶液,溶液变化,说明溶液中含有Fe2+
D.向硫酸亚铁铵溶液中,依次加入氯水和硫氰化钾溶液,溶液变化,说明溶液中含有Fe2+
8.下列叙述不正确的是 ( )
A.电解饱和食盐水时,用铁作阳极,Cl-发生氧化反应
B.电解法精炼铜时,纯铜作阴极,Cu2+发生还原反应
C.电镀铜时,金属铜作阳极,电镀液可用硫酸铜溶液
D.铜锌原电池中,锌作负极,电子从锌极流向铜极
7.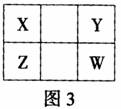 已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图3
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图3
所示,Y、W不是O族元素。下列说法正确的是 ( )
A.Z元素的原子半径可能比Y元素的小
B.Z元素的最高化合价可能比Y元素的高
C.W的气态氢化物的稳定性一定比Y的强
D.Z的最高价氧化物的水化物的酸性一定比W的强
6.下列说法正确的是 ( )
A.CO2、H2O都是非极性分子
B.乙酸、蔗糖都是弱电解质
C.C6H6O、C7H8O一定互为同系物
D.石英、食盐、金属钠、干冰的熔点依次降低
5.下列说法不正确的是 ( )
A.利用化学变化可以用活性炭除去冰箱中的异味
B.利用化学变化反应可以制得用作半导体材料的高纯硅
C.利用化学方法可以提高煤炭利用率,减少污染物的排放
D.利用高科技设备可以使人们清楚地观察到原子的图像和动态的化学变化
33.(8分)[化学一有机化学基础]
中国是《日内瓦协定书》缔约国,一贯反对使用化学武器,反对任何形式的化学武器扩散。苯氯乙酮是一种具有荷花香味的有强催泪性的杀伤化学毒剂,它的结构简式为
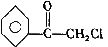 。苯氯乙酮的一种同分异构体有如下转化关系:
。苯氯乙酮的一种同分异构体有如下转化关系:

请写出:
(1)A、D的结构简式和X的化学式
A:_________;D: _________; X:_________;
(2)C→D的反应类型:_________
(3)A→B的化学方程式:__________________。
32.(8分)[化学一物质结构与性质]
据最新一期的《新科学》杂志报道,科研人员在20℃、1个大气压和其它一定的实验条件下,给水施加一个弱电场,水就可以结成冰,称为“热冰”。下图是水和“热冰”微观结构的计算机模拟图。回答:

(1)以上信息体现了水分子具有_________性,水分子中氧原子的杂化方式为_________。
(2)参照热冰的图示,以一个水分子为中心,画出水分子间最基本的连接方式(用结构式表 示)。
 (3)固体二氧化碳外形似冰,受热气化无液体产生,俗称“干冰”。根据右图干冰的晶胞的结构回答:
(3)固体二氧化碳外形似冰,受热气化无液体产生,俗称“干冰”。根据右图干冰的晶胞的结构回答:
①一个晶胞中有_____个二氧化碳分子;在二氧化碳分子中
所含的化学键类型与数目有是_______;在干冰中CO2的
配位数______。
① 其堆积方式与干冰晶胞类型相伺的金属有(答一种即可)
__________,其空间利用率为____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com