
28.(12分)A、B、C为三种不同短周期非金属元素的单质,化合物E其有漂白性;G分子由形成B、C两单质的两种元素组成,一个G分子中含有18个电子。A→H等物质之间相互转化的关系如下(反应生成的水略去):
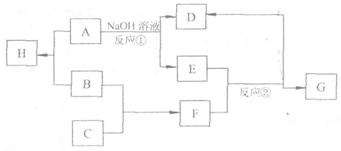
(1)若化合物H和F相遇生成固体X时,有白烟产生;则X的溶液中鉴定阳离子的实验方法和现象是
;
(2)反应①的离子方程式为 ;
反应②的化学方程式为 。
(3)若将1 L 0.2mol·L-1的X溶液和1L0.1 mol·L-1的NaOH溶液混合,则得到的溶液中有关离子和分子(H2O除外)的浓度由大到小的关系为 ;
和 两种粒子的物质的量之和比OH-多0.1 mol。
15.对室温下pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,有关叙述正确的是
A.加入适量的氯化铵晶体后,两溶液的pH均减小
B.温度下降10℃,两溶液的pH均不变
C.分别加水稀释10倍,两溶液的pH仍相等
D.用同浓度的盐酸中和,消耗的盐酸体积相同
第II卷(必做120分+选做32分,共152分)
第II卷共16大题,其中23-30题为必做部分,考生可用黑色签字笔、钢笔或圆珠笔直接将答案写在答题纸上:31-38题为选做部分,考生必须从中选择2个物理1个化学和1个生物题目作答,多选多做不计分。选做的题目,考生须将答案用黑色签字笔、钢笔或圆珠笔写在答题纸规定的位置,且必须标明题号。
[必做部分]
14.下列实验中金属或氧化物可以完全溶解的是
A.0.1 mol锌片投入到100 mL 1 mol·L-1的盐酸溶液中
B.1 mol MnO2粉末与400 mL10 mol·L-1的盐酸共热
C.常温下1mol铝片投入到200mL18.4mol·L-1硫酸中
D.常温下 1 mol铜片投入含4molHNO3的浓硝酸中
13.关于下列各装置图的叙述中,不正确的是

A.装置①中,c为阳极、d为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
12.下列反应的离子方程式正确的是
A.NaHCO3溶液中加入盐酸:CO32-+2H+=CO2↑+H2O
B.紫色石蕊试液中滴入氢硫酸变红的原因是:H2S 2H++S2-
2H++S2-
C.将NaHSO4溶液滴入Ba(OH)2溶液中至pH=7:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
D.电解CuSO4溶液:Cu2++2H2O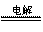 Cu+O2↑+4H+
Cu+O2↑+4H+
11.下图是198 K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是
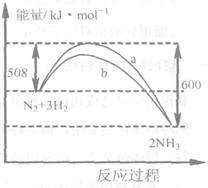
A.该反应的热化学方程式为:N2+3H2 2NH3 △H=-92
kJ·mol-1
2NH3 △H=-92
kJ·mol-1
B.向一密闭容器中加入1 mol N2和3 mol H2充分反应后,放出92 kJ热量
C.b曲线是加入催化剂时的能量变化曲线
D.加入催化剂可增大正反应速率,降低逆反应速率
10.具有相同电子层结构的三种微粒An+、Bn-、C,下列分析正确的是
A.原子序数关系是C>B>A B.离子半径的关系是Bn-<An+
C.A、B能形成1:1型化合物 D.原子半径的关系是A<C<B
9.下列是某学生自己总结的一些规律,其中正确的是
A.氧化物不可能是还原产物,只可能是氧化产物
B.有些化学反应不属于化合、分解、置换、复分解中的任何一种反应
C.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
D.将Mg(HCO3)2溶液加热,最终得到Mg(OH)2沉淀,由此可知KSP[Mg(OH)2]>KSP(MgCO3)
33.(8分)[化学--有机化学基础]
2005年诺贝尔化学奖授予在烯烃复分解反应研究领域有卓越贡献的三位法、美化学家。烯烃复分解反应实现了有机物碳碳双键两边基团的换位。如:
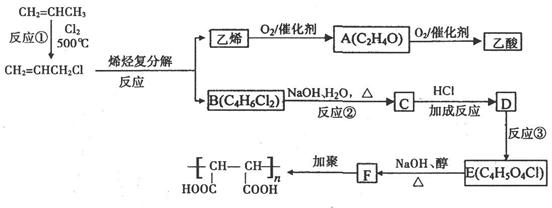
2CH2=CHCl CH2=CH2+ClCH=CHCl
CH2=CH2+ClCH=CHCl
又知羟基在链端的醇在一定条件下可直接氧化为羧酸,E是一种氯代二元羧酸。
现以丙烯为主要原料合成乙酸和聚合物
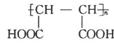
回答以下问题:
(1)写出下列结构简式:A ,B 。
(2)写出反应类型:反应① ,反应② ,反应③ 。
(3)不是由C直接转化为F,而是C先与HCl加成,这一步的目的是 。
(4)完成E→F的化学方程式 。
32.(8分)[化学--物质结构与性质]
分子(或离子)的空间构型有直线形、角形、平面形、四面体形、三角锥形等。为了解释和预测分子的空间构型,科学家在归纳了已知分子的空间构型的基础上,提出一种简单的理论模型,其理论依据是:分子中的价电子对(包括成键电子对和孤对电子)由于相互排斥作用,而取向彼此远离以减小斥力,分子尽可能采取对称的空间构型。对于ABm形分子(A为中心原子,B为配位原子),分子中的价电子对数(n)可以通过下式确定:
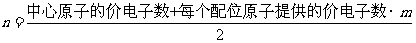
|
分子构型 |
AB2 |
AB3 |
AB2 |
AB3 |
AB4 |
|
价电子对数 |
2 |
3 |
4 |
4 |
4 |
|
几何构型 |
直线形 |
平面形 |
角形 |
三角锥形 |
四面体形 |
说明:①作为配位原子,氧原子、硫原子按不提供价电子计算;
②直线形分子中最少有3个原子,平面形分子中最少有4个原子。
(1)指出下面物质分子或离子的空间构型:PO43- ;CS2 ;AlBr3(共价分子) 。
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:

(3)按要求写出第二周期非金属元素构成的中性分子的化学式:
平面形分子 ,三角锥形分子 ,四面体形分子 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com