
21.(10分)实验室里用二氧化锰和浓盐酸加热制取氯气,也可以利用反应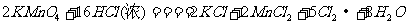 制取并收集纯净、干燥的氯气,部分装置如图所示:为
制取并收集纯净、干燥的氯气,部分装置如图所示:为
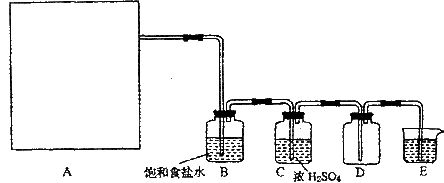
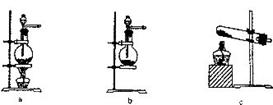
(1)用二氧化锰和浓盐酸制取氯气反应的离子方程式___________,若以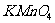 和浓盐酸为原料制取氯气,请根据反应原理从下图中选择合适的制气装置_______(填代号)。
和浓盐酸为原料制取氯气,请根据反应原理从下图中选择合适的制气装置_______(填代号)。
(2)装置B的作用是___________。
(3)E中的试剂应选用____________溶液,反应的离子方程式为____________
(4)某学生通过下列两种方式制取氯气:
①用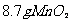 与足量浓盐酸反应制取
与足量浓盐酸反应制取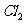
②用含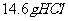 的浓盐酸与足量
的浓盐酸与足量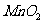 反应制取
反应制取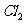 。这两种方式产生
。这两种方式产生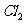 的量的关系是_________(填选项)。A.①多 B.②多 C.①②一样多
的量的关系是_________(填选项)。A.①多 B.②多 C.①②一样多
20.下列说法正确的是
A.金属元素的原子只有还原性,离子只有氧化性
B.原子最外层只有1个电子的元素一定是金属元素
C.最外层电子数比次外层电子数多的元素一定位于第二周期
D.原电池中排在金属活动性顺序表前面的金属总是作负极,排在后面的金属总是作正极
第Ⅱ卷(共50分)
19.A和M为两种元素,已知A位于短周期,且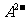 与
与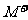 的电子数之差为8,则下列说法正确的是
的电子数之差为8,则下列说法正确的是
A.A和M原子的电子总数之和可能为1l
B.A和M的原子序数之差为8
C.A和M原子的最外层电子数之和为8
D.A和M原子的最外层电子数之差为7
18.在2L密闭容器内充入5 mol A和2.5
mol B使之发生反应;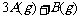


 ,经过5min反应达到平衡,经测定C的平均反应速率为
,经过5min反应达到平衡,经测定C的平均反应速率为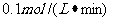 。
。
下列叙述中正确的是
A.恢复至原温度,容器内压强增大
B.A的平均反应速率为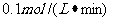
C.达到平衡时,B比A的转化率小
D.B的平衡浓度为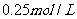
17.浓盐酸和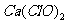 能发生如下反应:
能发生如下反应: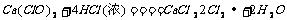 ,用贮存很久的漂白粉与浓盐酸反应制得的
,用贮存很久的漂白粉与浓盐酸反应制得的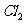 中,不可能含有杂质气体是
中,不可能含有杂质气体是
A.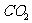 B.
B.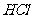 C.
C.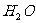 D.
D.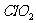
16.下列元素一定为主族元素的是
A.最外层有3个电子的元素
B.最高正价为+7价的元素
C.最外层只有1个或2个电子的元素
D.最高价氧化物对应水化物是酸的元素
15.现有甲、乙两种短周期元素,室温下甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。则下列说法不正确的是
A.甲、乙两元素相比较,金属性:甲<乙
B.将在空气中放置已久的这两种元素的块状单质分别放入热水中以此证明甲、乙金属性强弱
C.将这两种元素的单质粉末分别和同浓度的盐酸反应以此证明甲、乙金属性强弱
D.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液以此证明甲、乙金属 性强弱
14.可逆反应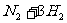


 的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
A. B.
B.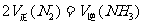
C.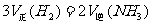 D.
D.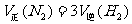
13.在人体所需的十多种微量元素中,有一种称为“生命元素”的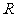 元素,对延长人类的寿命起着重要的作用。已知R元素的原子有四个电子层,其最高价氧化物分子式为
元素,对延长人类的寿命起着重要的作用。已知R元素的原子有四个电子层,其最高价氧化物分子式为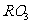 ,则
,则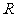 元素的名称为
元素的名称为
A.硫 B.砷 C.硒 D.硅
12.右图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子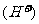 和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为
和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为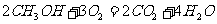 ,下列说法不正确的是
,下列说法不正确的是

A.左电极为电池的负极,a处通入的物质是甲醇
B.右电极为电池的负极,b处通人的物质是空气
C.甲醇失去电子被氧化
D.该装置将化学能转化为电能
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com