
20.(8分) 已知在0.1 mol/L的NaHSO3溶液中有关粒子浓度由大到小的顺序为:c(Na+)>c(HSO3-)>c (SO32-)>c (H2SO3)
(1) 则该溶液中c(H+)___________c(OH-)(填“<” “=” “>”),简述理由(用离子方程式表示) _________________________________________________________________。
(2) 现向NH4HSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是________________________________________________________,写出该反应的离子方程式____________________________________________________________。
19.(7分)某烧碱样品含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行如
下操作:
(1) 称量:在____________上准确称取烧碱样品W g,将其在烧杯中加适量水溶解。
(2) 配制物质的量浓度溶液:将溶解冷却后的碱液转入在250 mL___________中,洗涤、加水、定容,配制好250 mL烧碱溶液。
(3) 量取待测溶液:用配好的烧碱溶液润洗碱式滴定管后装入碱液,并从中放出25mL碱液于____________中,滴入2~3滴酚酞作指示剂。
(4) 装入标准酸液:将物质的量浓度为M mol/L的标准H2SO4溶液装入____________,调整液面,记下开始刻度数为Vl mL。
(5) 滴定,在锥形瓶底垫上一张白纸,当溶液颜色____________且半分钟内不恢复原色时停止滴定,记录此时酸液的体积读数为V2 mL。
(6) 计算:该烧碱纯度的计算式为____________________________________。
18.(7分) 用石墨作电极电解下列溶液①稀H2SO4 ②K2SO4溶液 ③NaCl
④CuSO4 ⑤KOH溶液
(1) 阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1的是(填序号)____________,它们阳极的电极反应式都是___________________________,总反应的化学方程式都是____________________________________________。
(2) 阴极、阳极都有气体产生,其中溶液pH变小的是____________(填序号)。
(3) 一个电极析出金属,一个电极逸出气体,且溶液pH明显减小的是____________(填序号),其总反应的化学方程式是_____________________________________________。
17.下面有关晶体的叙述中。不正确的是
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围紧邻距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻距离相等的Cl-共有8个
D.干冰晶体中,每个CO2分子周围紧邻l0个CO2分子
第Ⅱ卷 (非选择题 共49分)
16.蓄电池是一种可反复充电、放电的装置。它放电时起原电池的作甩,将化学能转变为电能;而充电时起电解池的作用,将电能转变为化学能贮存起来。某蓄电池充电和放电时发生的反应为: 。关于此蓄电池有下列说法:
。关于此蓄电池有下列说法:
①放电时,NiO2为正极;
②充电时,阳极反应式为: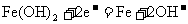 ;
;
③放电时,电解质溶液中的阳离子向正极方向移动;
④充电时,Ni(OH)2的反应式为: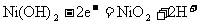 ;
;
⑤蓄电池的电极必须浸在碱性电解质溶液中;
其中正确的组合是
A.②③④ B.①②③ C.②④⑤ D.①③⑤
15.已知0.1 mol·L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等:
C.在NaHA溶液中一定有c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有c(Na+)>c(A2-)>c(H+)>c (OH-)
14.在常温时的下列溶液中,BaS04的溶解度最大的是
A.40 mL1 mol·L-1的BaCl2溶液 B.30 mL 2 mol·L-l的Ba(OH)2溶液
C.10 mL纯水 D.50 mL 0.1 mol·L-1的H2SO4溶液
13.物质的量浓度相同的下列溶液中,NH4+浓度最大的是
A.NH4Cl B.NH4HSO4 C.CH3COONH4 D.NH3·H2O
12.已知常温下某水溶液中由水电离出来的c(H+)=10-14mol/L,溶液中可能含有 ①Fe2+ ②Cl- ③HCO3- ④Na+ ⑤NO3- ⑥Al3+,上述离子肯定能在该溶液中大量共存的是
A.①②④ B①③⑤ C.②④⑤ D.③④⑥
11.反应2X(g)+Y(g)==2Z(g) △H<0 在不同温度和压强下,产物A的物质的量与反应时间的关系如图所示。则下列叙述正确的是
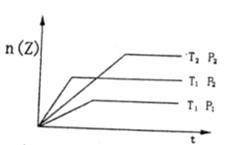
A.T1>T2,Pl<P2 B.T1>T2,Pl>P2 C.T1<T2,Pl>P2 D.T1<T2,Pl<P2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com