
21.(9分)某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素,选用的试剂如下:镁条、铝条、铝粉、钠、新制的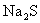 溶液、新制的氯水、0.5mol/L的盐酸、3mol/L的盐酸、酚酞试液,其设计的实验方案及部分实验现象如下表:
溶液、新制的氯水、0.5mol/L的盐酸、3mol/L的盐酸、酚酞试液,其设计的实验方案及部分实验现象如下表:
|
实验步骤 |
实验现象 |
|
①将一小块金属钠放人滴有酚酞试液的冷水中 |
钠块浮在水面上,熔化成闪亮的小球,做不定向移动,随之消失,溶液变红色 |
|
②将表面积大致相同的镁条和铝条(均已用砂纸打磨过),分别投入足量的相同体积的0.5mol/L的盐酸中 |
镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快 |
③将新制的氯水滴加到新制的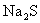 溶液中 溶液中 |
|
|
④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol/L的盐酸和3mol/L的盐酸中 |
剧烈反应产生气体,但铝粉消失比镁条快 |
请回答下列问题:
(1)实验③的现象是 ,该反应的离子方程式为 。
(2)由实验③得出的实验结论是 ,
(3)由实验②可得出决定化学反应快慢的主要因素是 ,
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确? (填是或否)
(5)通过实验④说明要加快化学反应速率可 或 。
22.(9分)目前世界上60%的镁是从海水中提取的。学生就这个课题展开了讨论。已知海水提镁的主要步骤如下:
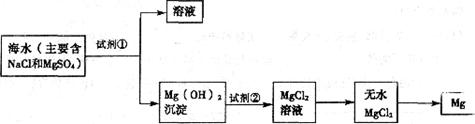
学生就这个课题提出了以下问题:
20.在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是
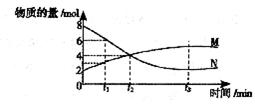
A.反应的化学方程式为: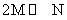
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率等于逆反应速率
D.t1时,N的浓度是M浓度的2倍
第Ⅱ卷(非选择题共50分)
19.A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3︰4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述不正确的是
A.X、Y、Z的稳定性逐渐减弱
B.A、B、C、D只能形成5种单质
C.X、Y、Z三种化合物的熔沸点逐渐升高
D.自然界中存在多种由A、B、C、D四种元素组成的化合物
18.短周期元素X、Y的原子序数相差2。下列有关叙述正确的是
A.X与Y不可能位于同一主族
B.X与Y一定位于同一周期
C.X与Y可能形成共价化合物XY
D.X与Y可能形成离子化合物XY
17.某研究性学习小组为了探究镁粉与溴水反应的机理,做了如下四种实验:
①将镁粉投入到冷水中,未观察到明显现象;
②将镁粉投入到溴水中,观察到只是开始时产生极少量的气泡,但溴水会慢慢褪色;
③将镁粉投入到液溴中,未观察到明显现象;
④向含有足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去。
下列关于镁粉与溴水的反应机理的叙述中正确的是
A.镁粉只直接与溴水中的溴反应
B.镁粉只与溴水中的酸反应
C.产生极少量的气泡是由于镁粉与水反应得到的
D.镁粉在水的催化下与溴发生反应
16.将纯锌片和纯铜片按图所示插入相同浓度的稀硫酸中,以下有关叙述正确的是
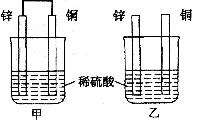
A.甲装置中电能转化为化学能
B.乙装置中电能转化为化学能
C.甲装置中铜片表面有气泡产生
D.乙装置中铜片表面有气泡生成
15.下列化学用语的书写,正确的是
A.氮气分子的电子式: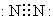
B.硫原子的结构示意图: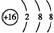
C.溴化钠的电子式: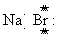
D.水分子的结构式:
14.某学生进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖。他的操作如下:取少量纯蔗糖加蒸馏水配成溶液;在蔗糖溶液中加入3-5滴稀硫酸;将混合液煮沸几分钟、冷却;在冷却后的溶液中加入银氨溶液,在水浴中加热。实验结果没有银镜产生。其原因是
A.蔗糖尚未水解
B.蔗糖水解的产物中没有葡萄糖
C.加热时间不够
D.煮沸后的溶液中没有加碱,以中和作催化剂的酸
13.天然气和液化石油气(主要成分为C3~C5的烷烃)燃烧的化学方程式表示为:


现有一套以天然气为燃气的灶具,今改为用液化石油气为燃料,应采取的正确的措施是
A.增大空气进入量,增大石油气进入量
B.减小空气进入量,减少石油气进入量
C.增大空气进入量,减少石油气进入量
D.减小空气进入量,增大石油气进入量
12.把氢氧化钠溶液和硫酸铜溶液加入某病人的尿液中,加热时如果观察到红色沉淀,说明该尿液中含有
A.食醋 B.葡萄糖 C.白酒 D.蛋白质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com