
6.等质量的下列烃完全燃烧,消耗氧气的量最少的是
A.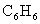 B.
B.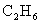 C.
C. D.
D.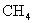
5.下列物质中,不属于高分子化合物的是
A.酶 B.油脂 C.淀粉 D.天然橡胶
4.医学研究证明,用放射性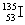 治疗肿瘤可收到一定疗效。下列有关,
治疗肿瘤可收到一定疗效。下列有关,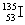 的叙述中,正确的是
的叙述中,正确的是
A.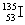 是碘的一种同素异形体
是碘的一种同素异形体
B.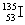 是一种新发现的元素
是一种新发现的元素
C.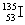 位于元素周期表中第5周期VIIA族
位于元素周期表中第5周期VIIA族
D.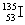 核内的中子数与核外电子数之差为26
核内的中子数与核外电子数之差为26
3.几种微粒具有相同的核电荷数,则可说明它们
A.可能属于同种元素 B.一定是同种元素
C.核外电子数一定相同 D.化学性质一定相同
2.下列叙述中,不会使蛋白质性质发生改变的是
A.动物的皮经过药剂鞣制后,变成柔软坚韧的皮革
B.打针时用医用酒精消毒
C.蛋白质溶液加入食盐变浑浊
D.用福尔马林溶液浸泡动物标本
1.元素的化学性质主要决定于原子的
A.质子数 B.中子数 C.核外电子数 D.最外层电子数
25.(6分)已知反应FeO(s) + CO(g)  Fe(s) + CO2(g) 的K=0.5(1273K)。若起始浓度c(CO)= 0.05 mol·L-1, c(CO2)= 0.01 mol·L-1,则
Fe(s) + CO2(g) 的K=0.5(1273K)。若起始浓度c(CO)= 0.05 mol·L-1, c(CO2)= 0.01 mol·L-1,则
(1)反应物、生成物的平衡浓度各是多少?
(2)CO的转化率是多少?
24.(5分)水的电离平衡曲线如图所示:
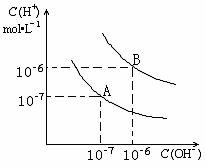
(1)若以A点表示25℃时水的电离平衡时的离子浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将pH= 8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为 。
23.(10分)如下图(a)为持续电解饱和CaCl2水溶液的装置(以铂为电极,A为电流表),电解一段时间后,从图(b)1小时起将CO2连续通入电解液中,请在图(b)中完成实验(a)中电流对时间的变化关系图,并回答有关问题。
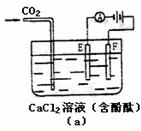
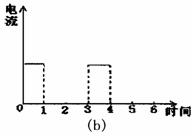
(1)完成实验(a)中电流对时间的变化关系图。
(2)电解时F极发生 反应,电极反应式为 ________ ;
E极的电极反应式为 ___________ ;电解的总化学方程式为 _______________________ 。
(3)电解池中产生的现象:①
② ③ 。
22.(8分)某种胃药片的制酸剂为碳酸钙,其中所含的CaCO3质量的测定如下, ①需配制0.1mol·L-1的HCl和0.1mol·L-1的NaOH溶液; ②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20.00mL蒸馏水; ③以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定,需用去VmL恰好完全反应; ④加入25.00mL0.1mol·L-1的HCl溶液。
(1)为使测定结果准确,至少需要滴定两次。写出全部实验过程中,各步操作的正确顺序(填编号):______________ _____________。
(2)配制0.1mol·L-1的HCl溶液和0.1mol·L-1的NaOH溶液需要的玻璃仪器除量筒、容量瓶外,还需要的有____________ _(填仪器名称)。
(3)写出有关的化学方程式_____ 。
(4)每片胃药中含碳酸钙的质量是 g(假设滴定过程中消耗NaOH溶液的平均体积为VxmL)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com