
1.请你运用所学的化学知识判断,下列有关化学观念的叙述错误的是 ( )
A.几千万年前地球上一条恐龙体内的某个原子,可能在你的身体里
B.用斧头将木块一劈为二,在这个过程中个别原子恰好分成更小的微粒
C.一定条件下,金属钠可以成为绝缘体
D.一定条件下,水在20℃时能凝固成固体
21(12分)下表中的实线表示元素周期表的部分边界。①-⑧分别表示周期表中对应位置的元素。
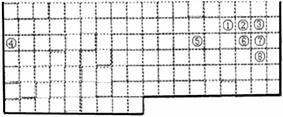
(1)请在表中用实线补全元素周期表的边界。
(2)元素周期表体现了元素周期律,元素周期律的本质是
。
(3)元素③④⑤⑥的原子半径由大到小的顺序是: ,元素⑤、⑥的最高价氧化物对应的水化物的酸性强弱为: > ( 用化学式表示)。
(4)元素③⑦⑧的氢化物的稳定性由高到低的顺序为: ( 用化学式表示)。
(5)元素①的氢化物的电子式为 ,其空间构型为 。
(6)元素⑤与⑦形成的化合物有净水作用,写出其与水作用的离子方程式: 。
22(4分)铜与浓硝酸反应和铜与稀硝酸反应,产物不同,实验现象也不同。 分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学乙提出这可能是Cu2+浓度差异引起的,你是否同意这种看法?
(填“同意”或“不同意”),原因是 ;另一同学甲提出溶液呈“绿色”是Cu2+与NO2混合的结果,现对铜片与浓硝酸反应后所得溶液进行了如下实验,能证明甲同学说观点正确地是 (填字母)
A加热,观察溶液颜色是否变化,发现变色
B加水,观察溶液颜色是否变化,发现变色
C 通入二氧化氮,观察溶液颜色是否变化,发现变色
D通入氧气,观察溶液颜色是否变化,发现变色
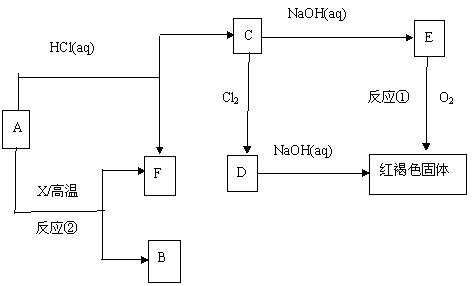 23(6分) 已知A为金属单质,它们之间能发生如下反应(部分产物未标出)
23(6分) 已知A为金属单质,它们之间能发生如下反应(部分产物未标出)
请根据以上信息回答下列问题:
(1)写出物质B、D的化学式:
(2)写出下列反应的化学方程式:反应①
反应②
24(12分)A、B、C、D均为中学所学的常见物质且均含有同一种短周期元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
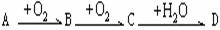
(1) 若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,且D为强电解质,
则A、D分别为(填写化学式)A: ,D: 。
写出A→B转化的化学方程式: 。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红。则A为 (填写化学式),写出A→B转化的化学方程式:
(3)若A为周期表中短周期元素形成的金属单质,D为强碱,则A元素位于周期表的 族,写出C→D转化的离子反应式: 。
(4)若A为短周期元素形成的非金属单质,除(1)、(2)中涉及到的元素外,请另外写出一种B→C转化的化学反应方程式 。
25(12分)实验室制取SO2的反应原理为:Na2SO3+H2SO4(浓) Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
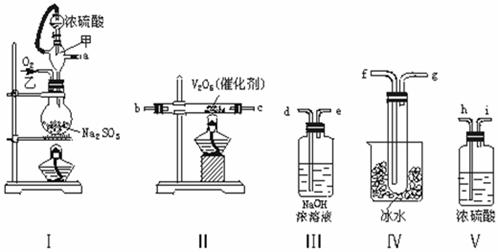
(1)这些装置的连接顺序(按气体左右的方向)是 → → →
→ → → → (填各接口的编号)。
(2)实验时Ⅰ装置中橡皮管的作用是 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。
(4)Ⅳ处观察到的现象是 。
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会 (填“增大”“不变”或“减小”)。
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为 。
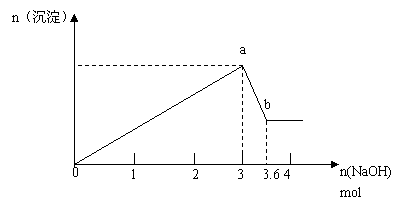 26(4分) 现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,请计算出FeCl3、AlCl3的物质的量浓度各为多少?
26(4分) 现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,请计算出FeCl3、AlCl3的物质的量浓度各为多少?
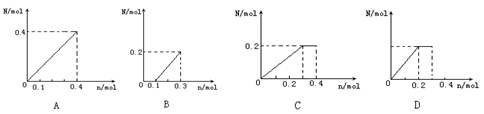
20.将0.4 mol铁粉逐渐加入到含硝酸0.8 mol的稀硝酸中,反应生成气体的物质的量N随消耗铁粉的物质的量n变化关系正确的是( )
Ⅱ卷(共50分)
19.已知质量分数为0.05的氨水溶液的物质的量浓度为amol·L-1,将这种氨水溶液稀释为质量分数为0.025的氨水溶液的物质的量浓度为bmol·L-1,则( )
A.a>2b B.a=2b C.a<2b D.无法判断
18.密闭容器中装有1mol NaHCO3和0.8mol Na2O2,加热充分反应后,容器内残留的固体是( )
A.0.8molNa2CO3和0.6molNaOH B.0.5molNa2CO3和1molNaOH
C.0.8molNa2CO3和1molNaOH D.1molNa2CO3和0.6molNaOH
17.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是( )
|
|
现象 |
解释 |
|
A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
Cl2能与淀粉发生显色反应 |
|
B |
浓HNO3在光照条件下变黄 |
浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
|
C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
说明该溶液中含有SO42- |
|
D |
铜片放入浓硫酸中,无明显变化 |
说明铜在冷的浓硫酸中发生钝化 |
16.能证明某溶液中含有Fe2+的是( )
A.该溶液呈浅黄色
B.该溶液中加入NaOH溶液,生成白色沉淀并迅速变成灰绿色,最后变为红褐色
C.向该溶液中加入氯水,再滴入几滴KSCN溶液,呈红色
D.向该溶液中滴入几滴KSCN溶液变红色,再加入氯水颜色无明显变化
15.下列各组物质的稀溶液相互反应,把前者逐滴滴入后者与把后者逐滴滴入前者,所产生的现象不相同的是( )
A.AlCl3 和NaOH B.Na2CO3和CaCl2
C.NaHCO3和HCl D.NaCl和AgNO3
14.下列溶液中: ①石灰水 ②H2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液,不能区别SO2和CO2气体的是 ( )
A.只有① B.①③ C. ①②③⑤ D.②③④⑤
13.已知反应①2BrO3- + Cl2 =Br2 +2ClO3- ②5Cl2 + I2 +6H2O=2HIO3 +10HCl ③ClO3- +5Cl-+6H+=3Cl2 +3H2O,下列物质氧化能力强弱顺序正确的是( )C
A.ClO3->BrO3->IO3->Cl2 B.BrO3- >Cl2>C1O3->IO3-
C.BrO3->ClO3->Cl2>IO3- D.Cl2>BrO3->C1O3->IO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com