
1.随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了防止仲秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常加入抗氧化物质,下列不属于抗氧化物质的是 ( )
A.生石灰 B.还原铁粉 C.亚硫酸钠 D.维生素C
21.(10分)在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生反应的反应均为放热反应)。生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。已知,生成C1O3-离子的反应为:6Ca(OH)2+6C12 5CaC12+Ca(C1O3)2+6H2O。
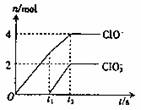
试回答:
(1)t2时,Ca(C1O)2与Ca(C1O3)2的物质的量之和为 mol,该石灰乳中含有的Ca(OH)2的质量是 g。
(2)据分析,生成Ca(C1O3)2的反应是由温度升高引起的,通过氯气的速度不同,C1O-和C1O3-的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后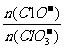 将 2(填“>”“<”或“=”);若
将 2(填“>”“<”或“=”);若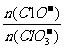 =a,则n(C1-)=
mol(用含a的代数式来表示)。
=a,则n(C1-)=
mol(用含a的代数式来表示)。
20.(11分)下图是部分化学常见的氧化物和单质的转化关系。其中。氧化物f是制造光导纤维的重要原料,氧化物c是一种具有磁性的黑色物质。回答下列问题:

(1)写出下列物质的化学式:单质C 氧化物d ;
(2)纯净的单质F在工业上的重要应用是 ;
(3)写出下列反应的化学方程式:
① ;
④ ;
⑤ 。
19.(12分)氯及其化合物是中学化学中的重要研究对象。
(1)写出实验室中制取氯气的离子方程式 ;
(2)实验室也可以利用如下反应制取氯气:KC1O3+6HC1(浓) KC1+3C12↑+3H2O。若制取标准状况下的6.72L氯气,该反应中电子转移的物质的量为
;
(3)某同学用排空气法收集一瓶氯气,进行氯气与铁反应的实验:取一根细铁丝 ,然后立即伸入充满氯气的集气瓶中,观察到的现象是 。为观察生成的氯化铁溶液的颜色,向反应后的集气瓶中加入少量的蒸馏水,振荡,实际观察到的现象是 ,产生这种现象的原因是 ;为真正观察到氯化铁溶液的颜色,应向反应后的集气瓶中改加(填试剂名称) 。
18.(6分)某同学取一张铝箔,并用针刺一些小孔,然后取一药匙过氧化钠粉末,用铝箔包好,放入下图所示装置倒扣的漏斗中。
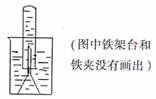
(1)按顺序写出该过程中发生反应的离子方程式:
①
② ;
(2)反应结束后,用拇指堵住试管口后将试管移出,靠近燃着的酒精灯,松开手指,观察到的现象是 。
17.(10分)一般测定样品中成分含量的实验应重复2-3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:
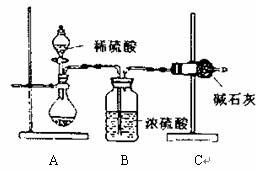
Ⅰ.甲同学的方案如上图所示:
(1)根据甲同学的实验装置图分析,在每次实验过程中所进行的称量操作至少要进行
次;
(2)甲同学重复测定了三次,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能的原因是 (填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收;
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收;
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收;
D.加入稀硫酸的量不足
Ⅱ.乙同学的方案是:从下图所提供的装置中选择实验装置,代替甲同学实验的B、C,通过测定放出的二氧化碳的体积(不考虑二氧化碳溶于水)来计算。
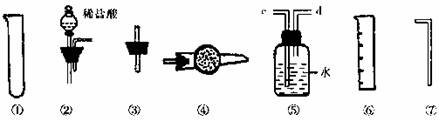
(1)选择最简装置的连接顺序为 ;
(2)产生的气体从装置⑤的 端进入。
Ⅲ.丙同学的方案是:称取样品mg,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体ng。
(1)混合物中碳酸钠的质量分数为(用m、n表示) ;
(2)Ca2+、Ba2+都可以使CO32-沉淀完全。乙同学能否使用氯化钙溶液代替氯化钡溶液?
为什么? 。
16.(6分)实验室需要配制0.5mol·L-1的烧碱溶液500mL,根据溶液配制的过程,回答下列问题:
(1)实验中除了托盘天平(带砝码)、药匙、量筒和玻璃棒外,还需要的其它玻璃仪器有: ;
(2)根据计算得知,所需NaOH固体的质量为 g;
(3)配制溶液的过程中,有以下操作。其中,正确的是 (填代号)。
A.将氢氧化钠固体放在纸片上称量;
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中;
C.将溶解氢氧化钠的烧杯中用蒸馏水洗涤2-3次,并将洗涤液转移到容量瓶中。
(4)玻璃棒在该实验中的作用有:①
。
②
。
15.在一定条件下,使CO和O2的混合气体26g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增重14g,则原混合气体中O2和CO的质量比可能是( )
A.9:4 B.1:1 C.7:6 D.6:7
|
14.在Fe2(SO4)3溶液中,加入ag铜,完全溶解后,再加bg铁,充分反应后得到cg残余固体,且a>c,则下列说法正确的是 ( )
A.残余固体是铜和铁
B.最后得到的溶液中一定含有Cu2+
C.将残余固体加入到稀H2SO4中,有气泡产生
D.最后得到的溶液中可能含有Fe3+
13.某溶液含有①NO3- ②HCO3- ③SO32- ④CO32- ⑤SO42- 等五种阴离子。向其中加入少量的Na2O2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积的变化)
( )
A.① B.①②④ C.①③⑤ D.①③④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com