
3.YBa2Cu8Ox(Y为元素钇)是磁悬浮列车中的重要超导材料,下列关于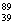 Y的说法中不正确的是
Y的说法中不正确的是
A.钇元素位于周期表第五周期
B.质子数与中子数之差为50
C.原子的核外电子数是39
D.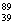 Y和
Y和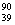 Y是两种不同的核素
Y是两种不同的核素
2.科学家经过不断的科学实验,初步获得了室温下水可以变成冰,不导电的塑料通过加入添加剂也能导电等科学认识。这说明
A.科学实验是人们获得认识的唯一途径
B.科学实验是人们认识的一个重要来源
C.科学实验是人类最基本的实践活动
D.科学实验是认识的最终目的
1.2007年3月温家宝总理在十届全国人大五次会议上提出“要大力抓好节能降耗、保护环境”,下列举措与这一主题不吻合的是
A.用“绿色化学”工艺,使原料完全转化为产物
B.推广燃煤脱硫技术,防治SO2污染
C.推广垃圾的分类存放、回收、处理
D.大量使用农药化肥提高粮食产量
25.(8分)在25℃时,用石墨电极电解100mL,1 mol·L-1AgNO3溶液。如有0.2mol电子发生转移,试回答下列问题:
(1)阴极上发生的电极反应为 ;
(2)电解后溶液中溶质的物质的量浓度为 (假设溶液的体积不变);
(3)计算电解产生的气体的总体积(标准状况)。
24.(11分)某研究性学习小组设计了如图所示的定量测定装置,其中B是底面积为100cm2、高20cm的圆筒状玻璃容器(带密封盖),上面标有以厘米为单位的刻度。其他夹持装置已略去。
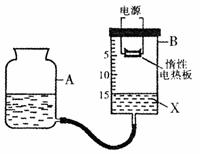
I.甲同学用这套装置测定出了空气中氧气的体积分数。他的操作过程是:①检查装置的气密性;②加入液体X(H2O),调整A的高度,使B中液面至刻度15.0cm处;③将过量的铁粉平铺在电热板上,盖紧容器;④通电加热铁粉,待充分反应后,冷却到原来的状况,调整A的高度使容器A、B中的液面保持水平,记录液面刻度。
请回答下列问题:
(1)在操作①中检查装置气密性的方法是
;
(2)在该同学的实验中,下列物质可代替铁粉的有 (填序号);
A.红磷 B.木炭 C.铜粉 D.镁粉
(3)在操作④结束时,装置B中的液面最接近的刻度是 cm(填整数)。
II.乙同学欲用此装置测定铁在氯气中燃烧产物的化学式。他的操作与甲不同之处是:将操作③中铁粉的质量改为1.0g,并向容器B中充满氯气(液面仍在15cm处)。
请回答下列问题:
(4)在乙同学的实验中,下列试剂适合于做液体X的有 (填序号);
A.水 B.氢氧化钠溶液 C.饱和食盐水 D.亚硫酸钠溶液
(5)实验结束时,液面在刻度8.8cm处。若实验条件看作标准状况,请据此计算生成物FeClx中x的值是 (计算结果保留1位小数);
(6)该实验结果与x的理论值有一定偏差,产生这种偏差的原因可能是(列举两条即可)
。
23.(7分)A~I是中学化学中的常见物质,其转化关系如下图所示(已略去部分反应条件):
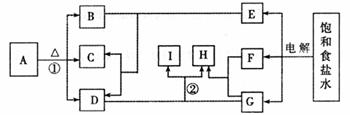
请回答下列问题:
(1)B的名称是 ,F的化学式是 ;
(2)反应①的化学方程式为 ;
(3)反应②的离子方程式为 ;
(4)除上述推断外,你认为A还可以是 (填化学式)
22.(7分)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40℃~50℃时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+ === Cu2++Cu。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是 (填“氧化剂”或“还原剂”);
(2)CuH在氯气中燃烧的化学反应方程式为 ;
(3)CuH溶解在稀盐酸中生成的气体是 (填化学式);
(4)如果把CuH溶解在足量的稀硝酸中只生成NO气体,请写出CuH溶解在足量稀硝酸中反应的化学方程式 。
21.(8分)A、B、C、D、E、F属于短周期主族元素。其中A元素原子是短周期中原子半径最大的原子,B是最小的原子;C元素原子的最外层电子数为m,次外层电子数为n;D元素原子的L层电子数为m+n,M层电子数为m-n;E元素原子的最外层电子数等于其电子层数,且在周期表中与D元素相邻;F元素原子的核外电子数是C元素原子的2倍。A、B、C三种元素可组成化合物X,C、D可组成化合物Y,C、E可组成化合物Z。
(1)写出下列元素的元素符号:B ,
D ,F ;
(2)A~F所形成的简单离子中,与Mg2+具有相同电子层结构的是 。(用离子符号表示);
(3)化合物Z与X的水溶液反应的离子方程式为 ;
(4)化合物Y用途广泛,试列举其中一种用途 。
20.(6分)已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物放出或吸收的热量叫该化合物的生成热。右图为氧族元素(钋除外)氢化物a、b、c、d的生成热数据示意图。
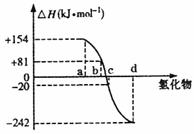
试回答下列问题:
(1)氧族元素中含18e-的两种氢化物的电子式为 、
;
(2)非金属元素氢化物的稳定性与生成1mol氢化物时的△H的关系为 ;
(3)硒化氢在热力学标准态下,发生分解反应的热化学反应方程式为 。
19.(7分)A、B、C、D均为中学化学所学的常见物质,且匀含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他产物已略去):
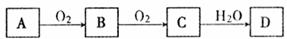
请填写下列空白:
(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,则D为(填写化学式)
;
(3)若A为气体,其水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红。则工业上合成A的化学方程式为 ;
(3)若A为短周期元素形成的非金属单质,则A可能是 。
(填3种不同单质的化学式)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com