
7.高压电机、复印机工作时会产生臭氧,该气体有强氧化性。下列叙述中不正确的是( )
A.臭氧和氧气是氧的同素异形体 B.臭氧的存在对人体有害无益
C.臭氧可使湿润的淀粉KI试纸变蓝 D.臭氧是很好的消毒剂和脱色剂
5.下列单质中,最容易跟氢气发生反应的是 ( )
A.F2 B.O2 C.Cl2 D.N2
|
①白磷保存在冷水中,②Na保存在CCl4中 ③HF溶液保存在塑料瓶中,④AgNO3固体保存在棕色试剂瓶内,⑤浓硝酸保存在溶液棕色广口瓶内
A.①③④ B.③④ C.①②③④ D.①②③④⑤
4.将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是 ( )
A.反应速率:两者相同
B.消耗硝酸的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
3.下列说法中正确的是 ( )
A.酸性氧化物都是非金属氧化物
B.含有极性键的分子一定是极性分子
C.含有离子键的化合物一定是离子化合物
D.所有物质中都存在化学键
2.2006年12月1日为世界第19个艾滋病日,调查结果显示全国艾滋病病毒感染者人数在不断地上升。医学界通过放射性14C标记的C60,发现C60的羧酸衍生物在特定条件下可断裂DNA杀死细胞,抑制艾滋病。关于14C的下列说法中正确的是 ( )
A.14C原子与C60中普通碳原子的化学性质不同
B.是C60的同素异形体
C.14C原子与14N原子所含中子数相同
D.与12C、13C是碳元素的三种同位素
1.我国科学家成功地合成了3mm长的管状碳纳米管,长度居世界之首。这种碳纤维具有强度高、刚度(抵抗变形的能力)高、密度小(只有钢的1/4)、熔点高,化学稳定性好的特点,因此被称为“超级纤维”。下列对碳纤维的说法中不正确的是 ( )
A.它是制造飞机的理想材料 B.它的主要组成是碳元素
C.它的结构与石墨相似 D.碳纤维复合材料不易导电
27.在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:
3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,通过计算完成下列问题:
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,通过计算完成下列问题:
(1)在该平衡下,在保持压强不变时,向该容器内充入氦气,则该平衡向 (填写“正向移动”、“逆向移动”、“不移动”)
(2)x的值为 ;
(3)平衡时A的转化率为 ;
(4)如果加入0.2mol的C、 0.2molD、0.9molB和0.7molA充入到原来容器内,保持原来的条件不变,则达到平衡时B的物质的量浓度是 。
26.实验室用下图所示的装置制取溴化亚铁。其中,A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两只耐高温的瓷夹,其中共盛有56g细铁粉。实验开始时先将铁粉加热至600-700℃,然后将干燥、纯净的CO2气流通入D中,E管中的物质开始反应,不断地将d中的液溴滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
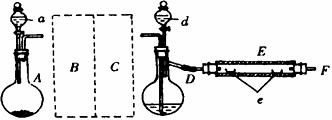
(1)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为 。
(2)在A中盛有CaCO3,a中盛有6mol·L-1盐酸。为使A中产生的CO2在进入D之前既干燥又纯净,B、C处采用相同的玻璃仪器,其仪器名称为 ;
B盛有的试剂是: ;C盛有的试剂是: .
(3)实验时,D和E的橡胶塞为什么最好用铝箔包住?
(4)反应过程中要不断地通入CO2,其主要作用是: 。
(5)E中在加热时进行的反应是:2Fe+3Br2=2FeBr3,2FeBr3=2FeBr2+Br2↑。此实验中溴化亚铁的产率为 。(保留到小数点后一位)
25.有常见A、B、C三种短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半。A元素原子最外层电子数比B元素原子最外层电子数多1个。甲是B元素含氧酸的钠盐。乙是C元素最高价含氧酸的酸式钠盐。丙是A元素含氧酸的钠盐(正盐)。甲、丙溶液pH>7,乙溶液pH<7,丁为气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间相互反应关系如下:
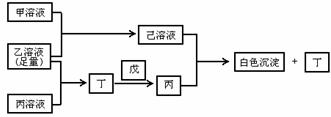
试回答:
(1)C元素原子结构示意图为: ;丁的结构式为: ;戊的电子式为: ;
(2)用有关离子方程式(或电离方程式)解释:
①乙溶液显酸性的原因是:_______________________________________;
②丙溶液呈碱性的原因是:_______________________________________;
(3)写出有关反应的离子方程式:
①乙溶液 + 丙溶液: ;
②己溶液 + 丙溶液: ;
24.根据所学知识完成下列空白:
(1)用惰性电极电解NaNO3溶液,要想恢复原来状态需要加入的物质 。
(2)用惰性电极电解CuSO4溶液的阳极反应式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com