
26.(7分)短周期元素A、B、C、D的原子序数依次增大,A、B同主族,A核外电子数等于其电子层数,C为元素周期表中原子半径最小的金属元素,D最外层电子数是其电子层数的3倍。填写下列空白。
(1)微粒半径比较:A- B+(填“>”、“<”或“=”)。
(2)A与D能组成化合物A2D和A2D2。A2D2的电子式为 。
A2D的沸点比D同主族其它元素与A组成的化合物的沸点高,原因是
。
(3)已知:在元素周期表中,有些元素的化学性质与其相邻左上方或右下方的另一主族元素的化学性质相似。则C构成的单质 (填“能”或“不能”)与强碱反应,B构成的单质在空气中充分燃烧,一定有或可能有的产物是 。
25.(8分)2007年2月27日某市工商局查获400克袋装中老年补钙营养奶粉1401包。这
种奶粉被鉴定为所含亚硝酸盐残留量高出正常值7.8倍,长期食用可能致癌。NaNO2有像食
盐一样的咸味。已知NaNO2能发生如下反应:2NaNO2
+ 4HI 2NO + I2
+ 2NaI+ 2H2O
2NO + I2
+ 2NaI+ 2H2O
(1)上述反应中氧化剂是 ,若有0.75mol的还原剂被氧化,则被还原的
氧化剂是 mol。
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可
选用的物质有:①自来水 ②碘化钾淀粉试纸 ③淀粉 ④白糖 ⑤食醋 ⑥白酒。进行实
验时,必须选用的物质有 。(填序号)
(3)某厂废切削液中,含2%-5%的NaNO2,直接排放会造成污染,下列试剂 (填
序号)能使NaNO2转化为不引起二次污染的N2。
①NaCl ②NH4Cl ③H2O2 ④浓H2SO4。
反应的化学方程式为: (并标出电子转移的数目和方向)。
24.(6分)贮气袋中贮有有色气体,可能由NO2、 CH4 、CO2、 HCl 、NH3 、Br2 (蒸气)等气体中的几种混合而成。现进行如下实验:
①通入少许水中,得无色溶液;
②通入少许AgNO3溶液中,有沉淀析出;
③通入少许澄清石灰水中,无浑浊现象;
④通过盛水的洗气瓶后,导出的气体再通入澄清的石灰水,石灰水变浑浊。
根据上述实验现象试判断:
该贮气袋中的气体一定存在 ,一定不存在 ,可能存在的是 。
23.现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互反应,图中每条连线两端的物质可以发生反应.下列判断不合理的是( )
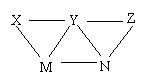 A.X一定是H2SO4
A.X一定是H2SO4
B.Y一定为K2CO3
C.Z可能为氯水
D.M、N必定各为BaCl2、FeSO4中的一种
第Ⅱ卷(共54分)
22.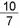 在标准状况下,将CO2和CO的混合气体(密度为 g/L)充满盛有足量Na2O2的密闭容器中(容积为22.4L),用间断的电火花引发至充分反应。反应完成后,对容器中的物质判断正确的是( )
在标准状况下,将CO2和CO的混合气体(密度为 g/L)充满盛有足量Na2O2的密闭容器中(容积为22.4L),用间断的电火花引发至充分反应。反应完成后,对容器中的物质判断正确的是( )
A.CO 0.5mol B.O2 0.125mol C.Na2CO3 0.25mol D.Na2CO3 0.5mol
21.有下列离子晶体的空间结构示意图。图中●和化学式中M分别代表阳离子,图中○和化学式中N分别代表阴离子,则化学式为MN2的晶体结构为( )

A. B. C. D.
20.硫酸铵在一定条件下发生反应:4(NH4)2SO4=== N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,将反应生成的混合气体通入到BaCl2溶液中,将会出现的现象是( )
A.无沉淀生成 B.生成BaSO4沉淀
C.生成BaSO3沉淀 D.生成BaSO4和BaSO3沉淀
19.已知C(s)+ O2(g)== CO2(g);△H =–393.5kJ•mol-1,2CO(g)+ O2(g)== 2CO2(g);△H =–566.0kJ•mol-1,则C(s)+ 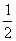 O2(g)== CO(g);△H为( )
O2(g)== CO(g);△H为( )
A.110.5kJ•mol-1 B.–110.5kJ•mol-1 C.172.5kJ•mol-1 D.–172.5kJ•mol-1
18.下列各组稀溶液,不用其它试剂或试纸,仅利用溶液间的相互反应,不能将它们区别开的是( )
A.KNO3、Na2SO4、CaCl2、BaCl2 B.H2SO4、Al2(SO4)3、NaCl、NaOH C.HCl、BaCl2、Na2CO3、NaOH D.NaHSO4、MgSO4、Na2CO3、NaOH
17.下列叙述与相应反应的离子方程式正确的是( )
A.少量的SO2通入到漂白粉溶液中:SO2 + Ca2+ + 2ClO- + H2O == CaSO3↓+ 2HClO
B.F2通入NaCl溶液中:F2 + 2Cl- == 2F- + Cl2
C.少量SO2通入过量的氨水中:NH3•H2O + SO2 == NH4+ + HSO3-
D.过量的CO2通入漂白粉溶液中:CO2 + ClO- + H2O == HCO3- + HClO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com