
17.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M。关于该反应的说法中正确的组合是( )
① 氧化剂是H3AsO3; ② 还原性:Cl->As;
③ 每生成7.5gAs,还原剂失去的电子为0.3 mol; ④ M为OH-;⑤ SnCl62-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
16.t℃时,将100 g某物质A的溶液蒸发掉10 g水,恢复至t℃,析出2.5 g晶体;再蒸发掉10 g水,恢复至t℃,析出7.5 g晶体。下列说法中正确的是( )
A.t℃时原溶液是饱和溶液 B.若A是CuSO4,则7.5 g晶体中含水2.7 g
C.t℃时A的溶解度为75 g D.原溶液中A的质量分数为40%
15.在c(H+)∶c(OH-)=1∶2的水溶液中能大量共存的离子组是( )
A.K+、Al3+、H2PO4-、SO42- B.Ca2+、NH4+、CO32-、Cl-
C.Na+、K+、NO3-、ClO- D.Na+、Ba2+、I-、SO32-
14.在Fe2(SO4)3溶液中,加入ag铜,完全溶解后,再加bg铁,充分反应后得到cg残余固体,且a>c,则下列说法正确的是( )
A.残余固体是铜和铁 B.最后得到的溶液中一定含有Cu2+
C.将残余固体加入到稀H2SO4中,有气泡产生 D.最后得到的溶液中可能含有Fe3+
13.下列物质之间的转化符合“甲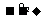 乙
乙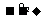 丙
丙 丁”的组合是(
)
丁”的组合是(
)
① Na→NaOH;② Cu→Cu(OH)2;③ S→H2SO4;④ CH3OH→HCOOCH3。
A.①③ B.②④ C.①②④ D.①③④
12.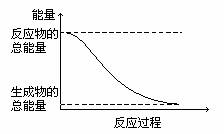 下列变化为放热反应的是( )
下列变化为放热反应的是( )
A.H2O(g)=H2O(l) △H=-44.0 kJ/mol
B.2HI(g)=H2(g)+I2(g) △H=+14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如右图所示的化学反应
11.下列叙述不正确的是( )
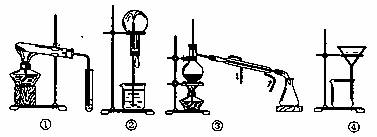
A.可用装置①鉴别碳酸钠和碳酸氢钠 B.可用装置②证明氨气极易溶于水
C.可用装置③从海水中得到淡水 D.可用装置④把胶体从溶液中分离出来
10.下列各组物质,都能与水反应且生成物都能溶于水的是( )
A.NH3、Cl2 B.Na2O2、SO3 C.NO、NO2 D.Mg、Al
9.下列离子方程式正确的是( )
A.二氧化硅与氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O
B.碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O
C.硫酸与氢氧化钡溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.铝与氢氧化钠溶液反应:Al +2OH-+2H2O=[Al(OH)4]-+H2↑
8.有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是( )
A.盐酸 B.烧碱溶液 C.氨水 D.KSCN溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com