
6、下列关于氯水的叙述正确的是( )
A.新制氯水中只含Cl2和H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡放出,该气体是Cl2
D.氯水长时间放置后pH将变大
5、下列叙述中错误的是 ( )
A、钠在空气中燃烧时发出黄色火焰
B、钠在空气中燃烧时生成氧化钠
C、钠可以与氯气发生化合反应
D、把钠放入氯化钠溶液中有化学反应发生
4、 下列关于研究物质性质的基本程序,排列顺序正确的是( )
①观察物质的外观性质 ②进行实验和观察
③做出有关的解释和结论 ④预测物质的性质
A、②①③④ B、①②③④ C、①④②③ D、④①②③
3、“绿色化学”是21世纪化学发展的主导方向。“绿色化学”要求从根本上消灭污染,是一门能彻底阻止污染产生的科学。它包括“绿色生产”和“绿色销毁”等内容。据报道,某地在整顿音像市场的活动中,查获了一大批盗版光盘,并进行了“绿色销毁”。以下做法中,属于“绿色销毁”的是( )
A. 泼上汽油焚烧 B. 倾倒入江河中
C. 深埋于土中 D. 碾压粉碎后再回收利用
2.化学是一门以实验为基础的自然科学,把化学元素及其化合物纳入一个统一的理论体系的著名科学家是( )
A.波义耳 B.门捷列夫 C.拉瓦锡 D.道尔顿
1、 化学科学的特征是( )
A、研究物质的变化 B、制造新物质
C、认识和制造分子 D、做实验
21.(17分)下图表示一个电解池,装有电解质溶液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
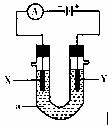
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①Y电极上的电极反应式 。
②在X电极附近观察到的现象是
。
(2)若X、Y都是惰性电极,a是浓度均为2mol·L-1的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后,X电极上有3.2g铜析出,写出电解过程中有关反应的离子方程式
,
此时直流电源已输出 mol电子。
(3)如果要用电解的方法精炼粗铜(含有Fe、Zn、Pt、C等杂质),电解质溶液a选用CuSO4溶液,则:
①X电极的材料是 ,电极反应式 。
②精炼完成后,硫酸铜溶液的浓度 (填“变大”、“变小”或“不变”)
(4)铅蓄电池反应的化学方程式是Pb+PbO2+2H2SO4=2PbSO4+2H2O。若以铅蓄电池为电源,用惰性电极电解CuSO4溶液,在电解过程中生成11.2LO2(标准状况),则铅蓄电池中消耗的硫酸的物质的量为 。
20.(12分)如下图,甲、乙、丙分别表示在不同条件下可逆反应:
 A(g)+B(g) xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
A(g)+B(g) xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
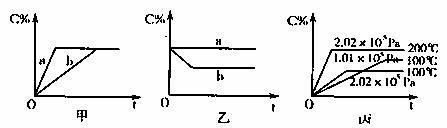
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况。
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入苛惰性气体后的情况,则 曲线表示恒温恒容的情况。
(3)根据丙图可以判断该可逆反应的正反应是 热反应(填“吸”或“放”),计量数x的值 (填取值范围);判断的依据分别是
。
19. (15分)已知2NO2(g) N2O4(g) △H(298K)=-52.7kJ·mol-1,某课外活动小组为探究温度和压强对化学平衡的影响,做了如下两组实验:
(15分)已知2NO2(g) N2O4(g) △H(298K)=-52.7kJ·mol-1,某课外活动小组为探究温度和压强对化学平衡的影响,做了如下两组实验:

I.该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到乙盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体。
请回答:
(1)A中的现象 ,B中的现象 。
(2)由此可知,降低温度,该化学平衡向 (填“正”或“逆”)反应方向移动。
(3)该化学反应的浓度平衡常数的表达式为 。升高温度,该反应中NO2的转化率将 (填“增大”、“减小”或者“不变”)。
II.在三支容积为30cm3针筒中分别抽入10cm3NO2气体,将针筒前端封闭。
(1)将第二支针筒活塞迅速推至5cm3处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深。
①推进针筒后颜色变深的原因是 ;
②一段时间后气体颜色又变浅的原因是 ;
③由此实验得出的结论是 。
(2)将第三支针筒活塞拉至20cm3处,该同学观察到的现象是
。
在此过程中,该反应的化学平衡常数将 ,NO2的转化率将 (填“增大”“减小”或“不变”)
18.(10分)2007年10月24日18时5分,“嫦娥一号”绕月卫星顺利发射升空。发射卫星的火箭使用的燃料是液氢和液氧。
(1)已知:H2(l)=H2(g) △H=akJ·mol-1
O2(l)=O2(g) △H=bkJ·mol-1
H2(l)+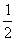 O2(l)=H2O(l) △H=ckJ·mol-1
O2(l)=H2O(l) △H=ckJ·mol-1
①气态氢和气态氧反应生成36g液态水时,反应的焓变是
(用含a、b、c、d的代数式表示);
②火箭使用液氢和液氧做燃料,除释放大量热和快速产生大量气体外,还有一个优点是 。
(2)2007年10月10日,诺贝尔化学奖授予德国科学家格哈德·埃特尔,以表彰他的固体表面化学研究领域取得的成就。其研究成果在燃料电池、气体在固体催化剂表面的反应等领域有着广泛的应用。
下图是氢氧燃料电池的示意图,回答下列问题:
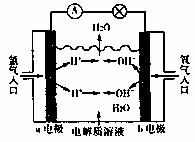
①若电解质溶液为稀硫酸,则电池的正极反应式为 ;
②若电解质溶液为KOH溶液,则电池的负极反应式为 ;
③现用该燃料电池做电源电解饱和食盐水,若在工作过程中消耗了32gO2,则可生产溶质质量分数为40%的NaOH溶液 g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com