
20.(10分)有A、B、C、D、E、F六种元素,试按下述所给条件推断:①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,原子半径A>B>C ②D、F是非金属元素,它们与氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的原子比D少一个电子层 ③F是地壳中含量最高的元素。请回答下列问题:
(1)写出A元素的名称___________,D位于周期表中第________周期________族,B的原子结构示意图为_____________________。
(2)A元素与F元素形成的AF型化合物中所含化学键类型为_______________________。
(3)写出E单质与A最高价氧化物对应的水化物反应的化学方程式:
_________________________________________________________。
(4)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式:
________________________________________________________________。
19.(16分)某化学课外小组设计了如下图所示的装置,进行氨气性质实验。利用图1完成氨的催化氧化实验,其中箭头表示气体流向,A、B表示两种纯净、干燥的气体,反应进行一段时间后,装置已中有红棕色气体生成。实验中所用的药品和干燥剂只能从下列物质中选取KMnO4、Na2O2、NH4Cl、NH4HCO3、P2O5、碱石灰、生石灰、蒸馏水、浓硫酸、浓氨水
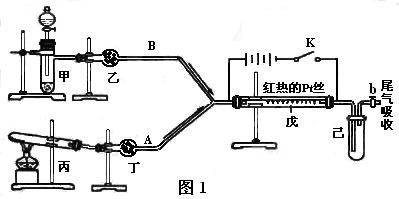
根据图I中装置和反应现象请回答:
(1)若乙中盛有P2O5,此时丙装置中发生反应的化学方程式为____________________。若丁中盛有P2O5,此时甲装置中应选择的试剂是____________________________。
(2)检验甲装置气密性的方法_________________________________________________
____________________________________________________________________________。
(3)当乙中充满红棕色气体后,停止甲、丙装置中的反应,并关闭a、b两个活塞,将己装置浸入冰水中,出现的现象是_______________________________________简述产生此现象的原因___________________________________________________________________
_______________________________________________________________________。
若将乙装置中的试管倒置于盛有水的水槽中,发生的现象是________________________。
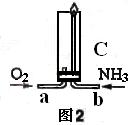
(4)已知氨气在纯氧中安静的燃烧,如图2,将过量O2与NH3分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气。先通入O2,后通过NH3的理由是
_____________________________________________________________________。
(5)液氨与水性质颇为相似,其电离方程式可表示为:2NH3 NH4++NH2-。某温度下其离子积常数为1×10-30(mol·L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
NH4++NH2-。某温度下其离子积常数为1×10-30(mol·L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
18.下列有关沉淀溶解平衡的说法正确的是( )
A.KSP(AB2)小于KSP(CD),则AB2的溶解度小于CD的溶解度
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大
C.在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动
第Ⅱ卷(非选择题 共56分)
17.以下为配制一定物质的量浓度的NaOH溶液的操作:①通过计算,将NaOH固体放在小烧杯中,用托盘天平称量所需质量 ②将称量的固体倒入小烧杯中,加适量蒸馏水溶解,用玻璃棒搅拌 ③冷却后用玻璃棒引流转移到容量瓶中,加水定容 ④摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线。其中错误的操作有( )
A.③④ B.②③ C.②④ D.①②
16.下列说法正确的是( )
A.氨氧化成一氧化氮的过程属于氮的固定
B.铝合金制作门窗是利用了其密度小、强度高等性质
C.硫酸铜晶体上滴加浓硫酸逐渐变白,利用了浓硫酸的脱水性
D.F、Cl、Br、I的氢化物稳定性逐渐减弱,其水溶液的酸性也逐渐减弱
15.下列各溶液中,微粒的物质的量浓度的关系正确的是( )
A.向硝酸钠溶液中滴加稀盐酸得到pH=5的混合溶液:c(Na+) = c(NO3-)
B.0.1mol·L-1Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+) + c(H2CO3)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.常温下,pH=7的NH4Cl与氨水的混合液:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
14.某温度下,容积一定的密闭容器中进行如下可逆反应:X(g) + Y(g) 2Z(g) +
W(s); △H>0,下列叙述正确的是( )
2Z(g) +
W(s); △H>0,下列叙述正确的是( )
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.平衡后,加入X,上述反应的△H增大
D.升高温度,平衡正向移动
13.我国首创的海洋电池以铝为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流,电池总反应为:4Al + 3O2 + 6H2O = 4Al(OH)3,下列说法正确的是( )
A.电池工作时,电流由铝电极沿导线流向铂电极
B.以网状的铂为正极,可增大与氧气的接触面积
C.为了增加海水的导电性,向海水中加入大量食盐
D.负极反应:O2 + 2HO2  4OH- - 4e
4OH- - 4e
12.在0.1mol·L-1的醋酸溶液中存在如下电离平衡:CH3COOH CH3COO- + H+,对于该平衡下列叙述正确的是( )
CH3COO- + H+,对于该平衡下列叙述正确的是( )
A.在该溶液中c(CH3COO-) = c(H+)
B.加水稀释后,溶液中所有离子浓度均减小
C.加入0.1mol·L-1的盐酸,溶液中的c(H+)增大
D.加入少量的CH3COONa固体,平衡向正反应方向移动
11.元素A和元素B的原子序数都小于18,已知A原子的最外层电子数为a,次外层电子数为b,B原子的M层电子数为(a-b),L层电子数为(a+b),则下列叙述不正确的是( )
A.B元素位于周期表中的第三周期、第IVA族
B.A、B两元素原子通过共价键形成的化合物BA2
C.A、B两元素所形成的化合物能与碳反应
D.A、B两元素所形成的化合物既能与氢氧化钠溶液反应又能与盐酸反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com