
7、下列各组溶液中所含溶质的物质的量相等,将其充分混合后不会产生沉淀的是
A、CaCl2、NaHCO3、KOH B、MgCl2、Ba(OH)2、HCl
C、FeCl3、H2S、HCl D、NaAlO2、K2CO3、NH3·H2O
6、现有碳酸钠、氢氧化钡、硫酸三种体积和物质的量浓度都相同的溶液,以不同的顺序将它们混合,如生成沉淀,立即过滤掉。关于所得溶液的酸碱性的下列结论中不正确的是
A、一定显碱性 B、可能显中性 C、不可能显酸性 D、可能显碱性
5、若溶液中由水电离产生的c(OH_)=10-14mol/L,满足此条件的溶液中一定可以大量共存的离子组是
A、Al3+、Na+、NO3-、Cl- B、Na+、K+、NO3-、Cl-
C、Na+、K+、Cl-、AlO2- D、NO3-、K+、NH4+、SO42-
4、下列离子方程式正确的是
A、碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
B、氯化铵与氢氧化钠两种浓溶液混合加热: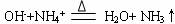
C、氢氧化镁与稀硫酸反应:H++ OH-= H2O
D、单质铜与稀硝酸反应:Cu+2H++2NO3-= Cu2++2NO↑+ H2O
3、将n molCu2S的与足量的稀硝酸反应,生成硝酸铜、硫酸、一氧化氮和水,则参加反应的硝酸中被还原的硝酸的物质的量是
A、4n mol B、10n mol C、10n/3 mol D、2n/3 mol
2、Na2O2、CaC2、CaH2、Mg3N2都能与水反应,且反应中都有气体放出。下列说法正确的是
A、都是氧化还原反应 B、CaC2, Mg3N2与水反应属于复分解反应
C、Na2O2,CaH2与水反应,水作氧化剂 D、CaH2与水反应产生H2,它是氧化产物
1、下列物质:①Cl2②Na ③Na2O2 ④NO2分别与水反应,氧化剂与还原剂的物质的量之比为1:1的是
A、 ①② B、②③ C、①②③ D、①②③④
23.(10分)2007年10月24日,我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥一号”探月卫星成功送入太空,迈出了向广寒宫求索的第一步。“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,第三级为液态氧燃料。
(1)常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-543kJ·mol-1
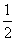 H2(g)+
H2(g)+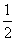 F2(g)=HF(g);△H=-269kJ·mol-1
F2(g)=HF(g);△H=-269kJ·mol-1
H2(g)+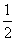 O2(g)=H2O(g);△H=-242kJ·mol-1
O2(g)=H2O(g);△H=-242kJ·mol-1
请写出肼和氟气反应的热化学方程式:__________________________________________。
(2)氢是一种理想的绿色能源,最近科学家利用太阳光分解水来制备氢。下图为光分解水制氢的循环系统,反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe2+等可循环使用。
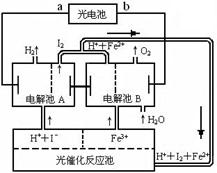
①判断光电池的a端为_________极,b端为________极。
②写出电解池A中电极反应式:
阴极______________________________,
阳极______________________________。
③电解池B中反应的离子方程式__________________________________________。
④若电解池A中生成H2的体积为8.96L(标准状况下),则电解池B中生成Fe2+的物质的量为____________________。
22.(9分)在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)  C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。请回答下列问题:
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。请回答下列问题:
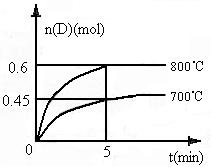
(1)700℃时,0-5min内,以B表示的平均反应速率为____________________________。
(2)能判断该反应是否达到化学平衡状态的依据是(多选扣分)__________________。
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)= c (c)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K=_______________,该反应为__________反应(填“吸热”或“放热”)。
(4)800℃时,某时刻测得体系中各物质的物质的量浓度如下:c(A)=0.06mol·L-1,c(B)=0.50mol·L-1,c(C)=0.20mol·L-1,c(D)=0.018mol·L-1,则此时该反应______________(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”)。
21.(11分)中学化学中几种常见物质的转化关系如下图所示:
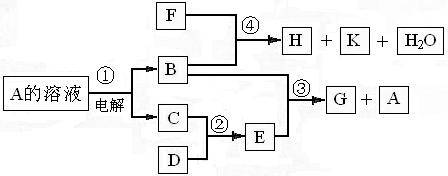
已知:B、C、D为常见单质,其中C为气休,B、D为金属;F为常见的强酸;K常温下为气体,且能使品红溶液褪色;将E溶液滴入沸水可制得一种红褐色胶体。
请回答下列问题:
(1)若用B作阳极,D作阴极,A溶液为电解质溶液,通电一段时间后,A溶液的pH_____(填“变大”、“变小”或“不变”)。
(2)写出反应③的离子方程式________________________________________________,反应④的化学方程式________________________________________________。
(3)写出检验G溶液中阳离子的方法____________________________________________
___________________________________________________________。
(4)实验中保存E溶液时要加入_____________________,用必要的文字和离子方程式解释原因_____________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com