
(二)若用98%(密度为1.84g/cm3)的浓硫酸稀释成3mol/L的稀硫酸100mL,回答下列问题: (1)需要取浓硫酸 mL
(2)由于错误操作,使得到的数据比正确数据偏小的是__________ (填写编号)。 A 用量筒量取一定量液体时,俯视液面读数 B 使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度 C 没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 D 容量瓶刚用蒸馏水洗净,没有烘干 E 定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 F 把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
19.现有A、B、C、D四种短周期元素,已知A、B同主族,B、C、D同周期,A、B的原子序数之和等于C、D的原子序数之和,C的单质能分别跟B和D的最高价氧化物的水化物反应。请回答:
(1)B和C的元素符号分别为 ;
(2)上述四种元素的原子半径由大到小的顺序(用元素符号表示)为 ;
(3)C单质与D的最高价氧化物的水化物反应的化学方程式为
写出C单质与二氧化锰在高温下反应的化学方程式,并标明电子转移的方向和数目。
(4)B跟D的最高价氧化物水化物的浓溶液发生氧化还原反应,生成的两种盐的水溶液均呈碱性,该氧化还原反应的离子方程式为
20、某无色溶液,可能由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干中组成。取该溶液进行以下反应:
(1)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
(2)在(1)所得溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
(3)在(2)所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。
(1)溶液中一定不存在的离子是______________________________________________;
(2)一定存在的离子是____________________________________________________;
(3)判断沉淀乙成份的方法是______________________________________________。
16、化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热能的形式表现出来,叫做反应热。由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等。
(1)许多化学反应的反应热可以直接测量,其测量的仪器叫做__________
(2)下列△H表示物质燃烧热的是_____________ ____;表示物质中和热的是___ _____ .
A. 2H2(g)+O2(g)=2H2O(l) ;△H1 B.C(s)+1/2O2(g)=CO2(g);△H2
C.CH4(g)+202(g)=C02(g)+2H2O(g) ;△H3 D.C(s)+02(g)=CO2(g);△H4
E.C6H12O6(s)+1202(g)=6CO2 (g)+6H2O (l) ;△H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H6
G.2NaOH(aq)+H2SO4(aq)=Na2S04(aq)+2H2O(l);△H7
H.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H8
(3) 甲硅烷 是一种无色液体,遇到空气能发生爆炸性自燃,生成
是一种无色液体,遇到空气能发生爆炸性自燃,生成 和水。已知室温下10g甲硅烷自燃放出热量446kJ,表示其燃烧热的热化学方程式为__________________。
和水。已知室温下10g甲硅烷自燃放出热量446kJ,表示其燃烧热的热化学方程式为__________________。
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1molCl2参与反应时释放145kJ的热量,写出这个热化学方程式: 。
(5)充分燃烧一定量的丁烷放出的热量为Q kJ,经测定完全吸收生成的二氧化碳需消耗5mol/L的KOH溶液100mL,恰好生成正盐。燃烧1mol丁烷放出的热量是
17、瑞香素是一种具有抗菌、抗炎、抗凝血等生物活性的香豆素化合物,其分子结构如图所示。回答下列问题。

(1)瑞香素的化学式为 。
(2)1 mol此化合物可与 mol Br2反应,
在一定条件下与H2反应时,最多消耗H2的物质的量为 mol。
(3)写出此化合物与强碱NaOH溶液反应的化学方程式:
。
18、(一)要配制500mL0.2mol·L-1的FeSO4溶液,实验操作步骤有:①在天平上称取ag绿矾(FeSO4·7H2O),将它放在烧杯中,用适量蒸馏水使其完全溶解 ②将所得溶液沿玻璃棒注入500mL容量瓶中 ③继续向容量瓶中加水至液面距刻度线1-2cm处,改用胶头滴管加蒸馏水至液面底部与刻度线相切 ④用少量水洗涤烧杯和玻璃棒2-3次,每次洗液都转入容量瓶 ⑤将容量瓶塞紧,充分摇匀 填写下列空白: (1)ag绿矾的实际质量为 g。 (2)上述操作步骤的正确顺序为 。 (3)若配制时遗漏步骤④,会使所配溶液的浓度 (填“偏高”、“偏低”或“无影响”)。 (4)若加蒸馏水是不慎超过刻度线,处理方法是 ;若操作步骤②时有溶液溅在容量瓶外,处理方法是 。
15、已知乙烯分子的所有原子在一个平面上。乙酸在一定条件下能生成一种重要的有机试剂M。核磁共振光谱发现M分子中的氢原子没有差别,红外光谱发现M分子里存在羰基,且M分子中所有原子在一个平面上。M极易与水反应重新变为乙酸,则M分子的结构简式可能是
A、(CH3CO)2O B、CH2==CO C、CH3CHO D、HCHO
14、下列关于Fe(OH)3胶体的说法中不正确的是
A、Fe(OH)3胶体与硅酸溶液混合将产生凝聚现象
B、Fe(OH)3胶体粒子在电场影响下将向阳极移动
C、液溶胶中Fe(OH)3胶体粒子不停地做布朗运动
D、光线通过Fe(OH)3胶体时会发生丁达尔现象
13、下列有关晶体的叙述中,不正确的是
A、金刚石网状结构中,有共价键形成的碳原子环中,最小的环上有6个碳原子
B、氯化钠晶体中,每个Na+周围距离最近且相等的Na+有6个
C、氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D、干冰晶体中,每个CO2分子周围紧邻12个CO2分子
12、科学家发现,不管化学反应是一步完成或分几步完成,该反应的热效应是相同的。已知在25℃,105 Pa时,1 mol C(石墨)完全燃烧生成CO2气体,放热393.5 kJ,1 mol CO完全燃烧生成CO2气体放热283.0 kJ,下列说法正确的是
A、在25℃,105 Pa时,C(石墨)燃烧生成CO气体的热化学方程式是:
2C(石墨) + O2(气) = 2CO(气) ;△H=-110.5 kJ/mol
B、C(石墨)不完全燃烧,生成CO2和CO混合气体时,放热283.0 kJ
C、C(石墨)和CO2(气)反应生成CO(气)的反应是吸热反应
D、如果金刚石的燃烧热大于石墨的燃烧热,则可以断定从石墨转变为金刚石的变化需要放热。
11、在标准状况下,1L的密闭容器中恰好可盛放n个N2分子和m个H2分子组成的混合气体,则阿伏加德罗常数可近似表示为
A.22.4(m+n) B.22.4×6.02×1023(m+n)
C.22.4(m+n)/(6.02×1023) D.m+n
10、某温度下将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的物质的量浓度之比为1︰3,则Cl2与NaOH反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
A.21︰5 B.11︰3 C.3︰1 D.4︰1,
9、从矿物学资料查得,一定条件下,自然界存在如下反应:
14CuSO4+5FeS2+12H2O==7Cu2S+5FeSO4+12H2SO4 下列说法正确的是
A、 Cu2S既是氧化产物又是还原产物
B、5mol FeS2发生反应,有10mol 电子转移转移
C、产物中的SO42-离子有一部分是氧化产物
D、FeS2只作还原剂
8、下列各组物质在溶液中的反应,可以用同一离子方程式表示的是
A. 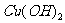 和盐酸,
和盐酸,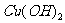 和醋酸
和醋酸
B. 
C.  和
和
D.  (过量)和
(过量)和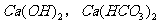 和
和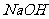 (过量)
(过量)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com