
5.下列实验操作正确的是( ).
①用带橡皮塞的棕色试剂瓶存放浓硫酸
②将0.1 mol·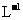 的NaOH溶液与0.5 mol·
的NaOH溶液与0.5 mol·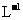 的
的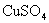 溶液等体积混合制得氢氧化铜浊液,用于检验醛基
溶液等体积混合制得氢氧化铜浊液,用于检验醛基
③实验室制硝基苯要在水浴的热水中插入温度计
④可用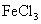 溶液除去试管内难以刷去的铜迹
溶液除去试管内难以刷去的铜迹
⑤用坩埚盛NaCl溶液加热制取NaCl晶体
A.①④ B.②④⑤ C.①③ D.③④
4.下列物质中,其水溶液能导电、溶于水时化学键被破坏,且该物质属于非电解质的是( ).
A.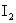 B.
B.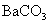 C.
C.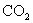 D.
D.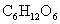 (葡萄糖)
(葡萄糖)
3.最近,意大利一所大学的科学家制造出了由4个氧原子构成的一种新型氧分子.若该氧分子具有空间对称结构,则下列说法正确的是( ).
A.该分子是氧元素的一种同位素 B.该物质与氧气互为同素异形体
C.该物质是一种氧化物 D.该分子是由极性键构成的极性分子
2.下列现象不是因为发生化学变化而产生的是( ).
A.皮肤不慎沾上浓硝酸而呈黄色
B.食盐撒在燃着的液化气火焰上,火焰呈黄色
C.久置的KI溶液呈黄色
D.盛在无色试剂瓶中的浓硝酸呈黄色
1.化工生产中尾气的排放是大气污染的主要因素,故在尾气排放前必须进行净化处理.下列工业废气经过处理后可作为燃料的是①硫酸工业尾气②硝酸工业尾气③高炉煤气④炼钢棕色烟气⑤炼油厂气( ).
A.①②③④ B.③④⑤ C.①③⑤ D.①②③④⑤
24.(8分)[化学-物质结构与性质]
A、B、C、D、E分别代表五种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素的M电子层达到p亚层中有3个电子,E与D同主族。
(1)C原子的电子排布式为 ;若A元素的原子最外层电子排布1s1,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于 键,A2C中C原子采取 杂化,D、E分别与元素A形成的化合物EA3的沸点____DA3的沸点(填“大于”“小于”或“等于”)
(2)当n=2时,B与C形成的晶体属于 晶体,BC2的空间构型为 ;
当n=3时,B与C形成的晶体中微粒间的作用力是 。
(3)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,则A、B、C、D四种元素的第一电离能由大小到小的顺序是
(用元素符号表示)。
23.(8分)[化学一有机化学基础]
下列有机化合物之间有如下的转化关系:
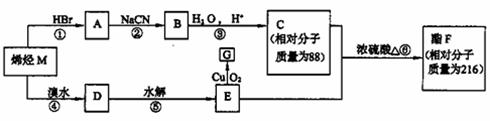
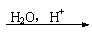 RCH2CN
RCH2COOH
RCH2CN
RCH2COOH
请根据以上框图回答下列问题:
(1)写出反应⑤的化学方程式 ;
(2)反应②的反应类型是 。
(3)物质E在铜作催化剂条件下被氧化生成G,1molG与足量银氨溶液反应生成单质银的物质的量为 mol;
(4)写出F可能的结构简式 、 。
22.(15分)830K时,在密闭容器中发生下列可逆反应:
 CO(g)+H2O(g) CO2(g)+H2(g) △H<0
CO(g)+H2O(g) CO2(g)+H2(g) △H<0
试回答下列问题:
(1)若起始时c(CO)=2mol·L-1,c(H2O)=3 mol·L-1,达到平衡时,CO的转化率为60%,则在该温度下,该反应的平衡常数K= 。
(2)在相同温度下,若起始时c(CO)=1 mol·L-1,c(H2O)=2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态
(填“是”与“否”),此时v(正) v(逆) (填“大于”“小于”或“等于”),你判断的依据是 。
(3)若降低温度,该反应的K值将 ,该反应的化学反应速率将
(均填“增大”“减小”或“不变”)
[选做部分]
21.(10分)某化合物M的化学式为C4H8O2,有如下转化关系,其中D是一种有强烈刺激性气味的无色液体,它是厨房中常用调味品的主要成分。
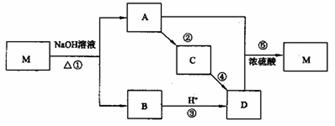
(1)写出反应①的化学方程式 ,
该过程中的主要反应属 反应;
(2)设计实验方案完成反应②的转化
。
(3)反应④属 反应。
(4)反应⑤的化学方程式为 ,该反应属 反应。
20.(9分)已各X、Y、Z都是短周期的非金属元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是外层电子数的三倍,X、Y和Z三元素可以形成一种强酸,X、Y和Z三元素还可以形成一种强酸盐。试填写下列空白:
(1)三种元素的名称分别是:
X. , Y. , Z. ;
(2)利用X和Z的单质、KOH溶液可组成燃料电池,负极的电板反应式为:
;
(3)由X、Y、Z所形成一种强酸盐,此盐在水溶液中显酸性的原因是(用有关离子方程式表示) ;
(4)X与Y形成的一种无色气体通常状况下的溶解度很大,写出该化合物与Z的单质在一定条件下(高温、催化剂)反应的化学方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com