
26.从海水中可提取各种化工原料,下图是工业上对海水的几项综合利用的示意图:

⑴在实验室进行过滤所需要玻璃仪器为______________。
⑵在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液。
则加入试剂的顺序是(填编号)______
⑶电解饱和食盐水时,与电源正极相连的电极上发生的反应为_______;与电源负极相连的电极附近溶液的pH_______(填“变大”、“变小”和“不变”)
⑷Mg(OH)2中加入盐酸后,要获得MgCl2·6H2O晶体,需要进行的实验操作依次为_____
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
⑸用相同电量分别电解无水MgCl2和饱和食盐水时,当生成1molMg的同时,生成NaOH的物质的量是________mol。
25. A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中有两种是气体;两种是固体。
回答:
(1)写出由B、C二元素所形成的原子个数比为1∶1的化合物的电子式__________,其晶体中存在的化学键有____________________(填化学键名称)。
(2)写出均由A、B、C、D四种元素组成的两种化合物的水溶液发生反应的离子方程式为____________________ 。
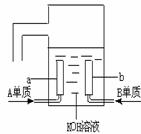
(3)用A元素的单质与B元素的单质可制成新型的化学电源,已在宇宙飞船中使用。其构造如图所示。两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。则a是 ___极,电极反应式为___________________。
24.对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25℃时有HA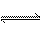 H++A-,则K=
H++A-,则K=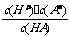 。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
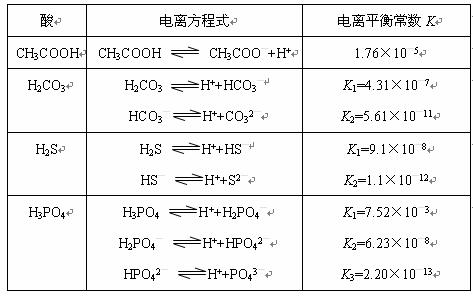
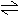
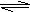 回答下列各题:
回答下列各题:
(1)K只与温度有关,当温度升高时,K值__________(填“增大”、“减小”、“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关 系?_____________________________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是_______,最弱的是_____________。
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是________________,产生此规律的原因是___________________________________。
23.(14分)某校化学兴趣小组的同学在进行研究性学习时,对“NO2能否支持燃烧”这个问题很感兴趣,他们决定自己动手设计实验进行探究。
(1)甲组同学设计的实验方案:向烧瓶中加入适量浓硝酸并加热,当烧瓶中有红棕色气体产生之后,将燃着的木条伸入烧瓶中,发现木条火焰熄灭。由此他们得出“NO2不能支持燃烧”的结论。
甲组同学所得的结论一定正确吗?请你说明理由:
。
(2)乙组同学通过查阅资料得知,一些不活泼金属的硝酸盐受热时也能产生NO2气体,如:2Cu(NO3)2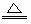 2CuO+4NO2↑+O2↑,2AgNO3
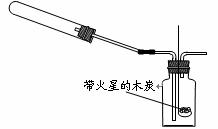
2CuO+4NO2↑+O2↑,2AgNO3 2Ag+2NO2↑+O2↑。他们根据此原理设计了如右图所示的实验装置(加热、夹持仪器未画出),并分别用Cu(NO3)2和AgNO3进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙组同学由此得出“NO2能支持燃烧”的结论。
2Ag+2NO2↑+O2↑。他们根据此原理设计了如右图所示的实验装置(加热、夹持仪器未画出),并分别用Cu(NO3)2和AgNO3进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙组同学由此得出“NO2能支持燃烧”的结论。
①老师认为上述两个实验中,有一个实验所得结论是不可靠的,你认为该实验中选用的反应物是 ,其结论不可靠的原因是 。
②运用该实验装置进行实验时,造成的不良后果是 。
(3)丙组同学拟设计一个用较为纯净的NO2气体(无O2产生)来探究“NO2能否支持
燃烧”的实验。
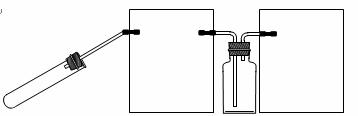
①丙组同学制取NO2的化学方程式是 。
②如图是该组同学设计的制取并收集NO2气体的实验装置,请在方框中将该装置补充完整,并注明补充装置中所用试剂。
22.为测定碳酸钙纯度(设含杂质SiO2),某学生研究性学习小组设计了如下几个实验方案:
[方案Ⅰ](1)称取碳酸钙样品m g(2)加入过量盐酸;
(3)收集并测定生成的气体体积V mL。
[方案Ⅱ](1)称取碳酸钙样品m g;(2)用c mol/L盐酸VmL(过量)溶解样品;
(3)取溶解后的溶液 mL,用c′mol/L
NaOH溶液滴定,恰好用去V′mL
mL,用c′mol/L
NaOH溶液滴定,恰好用去V′mL
[方案Ⅲ](1)称取碳酸钙样品m g;(2)高温(1000℃)煅烧直至质量不再发生变化,冷却后称量,质量为m′g。
[方案Ⅳ] (1)称取碳酸钙样品m g;
(2)加入足量c mol / L盐酸V mL使之完全溶解;
(3)过滤并取滤液;
(4)在滤液中加入过量c′mol/L Na2CO3溶液V′mL;
(5)将步骤(4)中的沉淀滤出、洗涤、干燥、称重为m′g。
回答下列问题:
(1)你认为上述4个方案中,最好的方案是 ,其他方案的缺点分别是:
方案 。
方案 。
方案 。
(2)为减少方案Ⅳ实验误差,必要的操作是 (填选项编号)。
A.精确测定Na2CO3溶液体积V′mL
B.精确配制浓度为c′mol/L Na2CO3溶液
C.将步骤(3)所得沉淀洗涤,洗涤液也应并入(4)中
21.下列是某兴趣小组研究浓硫酸的氧化性的结论并进行了实验验证:
①一般认为1:1的硫酸浓度大于60%,就具有一定的氧化性,越浓氧化性越强,60%以下的H2SO4氧化性就不怎么强了。
②温度也影响氧化性,如铜放于冷的浓硫酸中反应不明显,如果加热就可以观察到明显现象。
③98%的浓硫酸物质的量浓度为18.4mol·L-1,密度为1.84g·cm-3据以上信息回答:
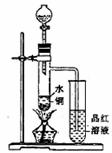
(1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓硫酸10-15滴(约0.5mL),加热至沸腾,该试管中液体是否有明显变化 _____。试用数据解释原因_________________________________。
(2)甲同学再用分液漏斗加浓硫酸10mL再加热至沸腾,现象是_____________________
_______________________________。
(3)乙同学利用所示装置直接从分液漏斗中加浓硫酸10mL与铜片反应。所观察到与甲不同的现象是______ ___________________原因是___________ _
_____________________。为了最终看到与甲类似的现象,乙同学需进行的操作是_______________________________________。
(4)乙同学进行加热,还在带支管的试管中观察到有黑色物质出现,大胆假设此物质是_______________。
20.“苏丹红一号”(结构如下图所示)是一种合成染料,科学家通过经毒理学研究,发现长期食用含有苏丹红的食品对人体可能有致癌因素。下列关于“苏丹红一号”的说法中不正确的是 ( )
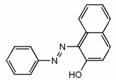
A.属于芳香族化合物,分子式为C16H12N2O
B.分子中的所有原子一定位于同一平面上
C.分子中苯环上的一取代物共有11种
D.能与NaOH溶液、FeCl3溶液、溴水等物质反应
|
19.将一定量的锌与l00 mL 18.5 mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6 L(标准状况)。将反应后的溶液稀释至1 L测得溶液中pH=1, 则下列叙述中错误的是 ( )
A.气体A为SO2和 H2的混合物 B.气体A中SO2和 H2的体积比为4∶l
C.反应中共消耗锌97.5 g D.反应中共转移电子3 mol
18.某温度下,在一容积可变的恒压密闭容器里,反应3A(g) 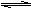 B(g) + 3C(g)达到平衡时,A、B和C的物质的量分别为6mol、2mol、6mol。在保持温度和压强不变的条件下,下列说法正确的是 ( )
B(g) + 3C(g)达到平衡时,A、B和C的物质的量分别为6mol、2mol、6mol。在保持温度和压强不变的条件下,下列说法正确的是 ( )
A.充入1 mol氦(He)(He与容器中气体不反应),平衡将向正反应方向移动
B.充入A、B、C各2 mol,平衡将向正反应方向移动
C.将A、B、C各减少1 mol,C的百分含量增加
D.加入一定量的A气体达平衡后,C的百分含量一定增加
17.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羧基硫(COS),已知羧基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法正确的是 ( )
A.羰基硫的属于非极性分子
B.羰基硫沸点比CO2低
C.羰基硫的电子式为: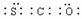
D.羰基硫分子中三个原子处于同一直线
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com