
18.不能通过化合反应制取的是: ( )
A.FeCl2 B.NaHCO3 C.H2SiO3 D.Fe(OH)3
17.将SO2气体通入BaCl2溶液至饱和,未见有沉淀生成,继续通入另一种气体仍无沉淀产生。则通入的该气体可能是: ( )
A.CO2 B.NH3 C.NO2 D.Cl2
16.如图所示甲、乙两个装置中,分别挤压胶头滴管向广口瓶中加入液体,两装置中的气球都明显地胀大(忽略液体体积对气球的影响)。则相应的胶头滴管和广口瓶中所用试剂可能是: ( )
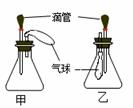
A.甲:NaOH溶液和CO2,乙:H2O2和MnO2
B.甲:CaCl2和Na2CO3溶液;乙:NaOH 溶液和Cl2
C.甲:浓硝酸和铝片,乙:溴水和二氧化硫
D,甲:浓硫酸和蔗糖,乙:水和氯化氢
15.用类推的方法可能会得出错误结论,因此类推出的结论要经过实践的检验才能确定其正确与否。下列类推结论中正确的是: ( )
A.工业上电解熔融MgCl2制取金属镁,工业上也用电解熔融AlCl3的方法制取金属铝
B.Mg失火不能用CO2灭火,Na失火也不能用CO2灭火
C.Al与S直接化合可以得到A12S3,Fe与S直接化合也可以得到Fe2S3
D.Fe3O4可以写成FeO·Fe2O3,Pb3O4也可写成PbO·Pb2O3
14.在标准状况下,向100 mL氢硫酸溶液中通人二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为: ( )
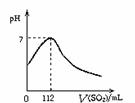
A.0.5 mol·L─1
B.0.05 mol·L─1
C.1 mol·L─1
D.0.1 mol·L─1
13.下列各种说法中错误的是: ( )
A.金刚石、石墨、C60是碳元素的同素异形体
B.目前人们发现了113种元素,但发现的原子种类数已大大超过了113种
C.二氧化硅在固态和熔融态时都不能导电
D.标准状况下,2.24 L SO3中,含硫原子数约为6.02×1022
12.下列各组气体或溶液用括号内试剂加以鉴别,其中不合理的是: ( )
A.二氧化碳、二氧化硫、一氧化碳(品红溶液)
B.氯化钠、硝酸银、碳酸钠(稀盐酸)
C.酒精、醋酸、醋酸钠(石蕊试液)
D.硫酸、硝酸钡、氯化钾(碳酸钠溶液)
11.下列叙述正确的是: ( )
A.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
B.加入稀盐酸,产生无色并能使澄清石灰水变浑浊的气体,原溶液一定有CO32─或SO32─
C.加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液一定有SO42─
D.元素的非金属性越强,其气态氢化物的稳定性越强,还原性越强
9.设NA表示阿伏加德罗常数的值,下列叙述中正确的是: ( )
A.在标准状况下,V L水含有的氧原子个数为(V/22.4)NA
B.0.2 mol过氧化氢完全分解转移的电子数目为0.4 NA
C.在常温常压下,17 g硫化氢所含质子数目为8 NA
D.在标准状况下,2.24 L二氧化硫与氧气混合气体中所含氧原子数为0.2 NA
|
①量取一定量液溴时,应在通风橱中小心吸取;
②容量瓶检漏:在容量瓶中按容量加足水,用手压紧瓶塞倒立1 min,如不渗漏,即可使用;
③测量溶液的pH时,应先将pH试纸润湿;
④用溴水除去乙烯中混有的二氧化硫气体;
⑤分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出;
⑥附着于试管内壁上的硫,可用热碱液洗涤;
⑦配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸。
A.只有②⑤⑦ B.只有①⑤⑥ C.只有①②⑤⑦ D.全部
8.下列实验不能达到预期目的的是: ( )
|
代号 |
实 验 |
实验目的 |
|
A |
Cl2、Br2分别与H2反应 |
比较氯与溴的非金属性强弱 |
|
B |
同温下测定相同浓度的Na2CO3和Na2SO4溶液的酸碱性 |
比较硫酸与碳酸的酸性强弱 |
|
C |
AlCl3、MgCl2溶液中通入过量氨气 |
比较镁与铝单质的还原性强弱 |
|
D |
同温下用同一电路分别测定同浓度的盐酸和某一元酸溶液导电能力 |
比较该一元酸与盐酸酸性的强弱 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com