
4.下列现象或应用不能用胶体知识解释的是 ( )
A.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
B.氯化铝溶液中加入小苏打溶液会产生白色沉淀和气体
C.牛油与NaOH溶液共煮,向反应所得的溶液中加入食盐有固体析出
D.水泥厂、冶金厂常用高压电除去工厂烟尘,减少对空气污染
3.在下列各说法中,正确的是 ( )
A.△H>0 kJ·mol-1表示放热反应,△H < 0kJ·mol-1表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5molO2反应放出的热就是H2的燃烧热
2.可以将反应Zn + Br2 = ZnBr2设计成蓄电池,下列4个电极反应 ( )
①Br2 +2e- == 2Br- ②2Br--2e-== Br2 ③Zn-2e-== Zn ④Zn2+ + 2e-==Zn
A.②和③ B.②和① C.③和① D.④和①
1.下列说法正确的是(NA为阿伏加德罗常数) ( )
A.124gP4含有P-P键的个数为4NA
B.12g石墨中含有C-C键的个数为3NA
C.12g金刚石中含有C-C键的个数为2NA
D.60gSiO2中含Si-O键的个数为2NA
33.(有机化学基础模块,15分)据报导,目前我国结核病的发病率有抬头的趋势。抑制结构杆菌的药物除雷米封外,PAS-Na(对氨基水杨酸钠)也是其中一种。它与雷米封可同时服用,可以产生协同作用。已知:
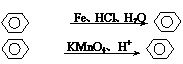 ①
-NO2
-NH2(苯胺、弱碱性、易氧化)
①
-NO2
-NH2(苯胺、弱碱性、易氧化)
② -CH3 -COOH
下面是PAS-Na的一种合成路线(部分反应的条件未注明)
A B
B C7H6BrNO2
C7H6BrNO2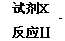
 C
C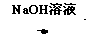 D
D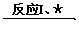 E
E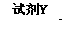
按要求回答问题:
(1)写出下列反应的化学方程式并配平:(7分)
A→B:_____________________________________________________;(4分)
B→C7H6BrNO2:_____________________________________________。(3分)
(2)写出下列物质的结构简式:C:_____________,D:______________。(4分)
(3)指出反应类型:I_____________________,Ⅱ___________________。(2分)
(4)指出所加试剂名称:X__________________,Y__________________。(2分)
32.(15分)某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(忽略N2O4的存在,图中铁架台等夹持仪器均已略去):
I.实验装置如下图所示(6分)
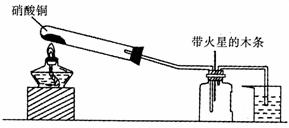
(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气。写出该反应的化学方程式_______________________________________________________________________
(2)当集气瓶中充满红棕色气体时,木条复燃了。有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确?_______(填“正确”或“不正确”),理由是_______ _
_______________________________________________________________________
II.实验装置如右图所示:(6分)
(1)写出浓硝酸受热分解的化学方程式:
__________________________________。(2分)
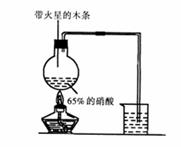 (2)实验开始后木条上的火星逐渐熄灭,有的同学提出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确?________(填“正确”或“不正确”),理由是
_________________。(4分)
(2)实验开始后木条上的火星逐渐熄灭,有的同学提出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确?________(填“正确”或“不正确”),理由是
_________________。(4分)
III.为了更能直接说明“NO2能否支持木条的燃烧”
这一问题,请你重新设计一个简单的实验方案,简述实验原理和主要操作。(3分)
31.(15分)已知A-I有如下图所示转换关系:
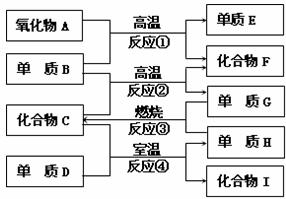
已知:①单质E可作为半导体材料;
②化合物F是不能生成盐的氧化物;
③化合物I能溶于水呈酸性,它能够跟氧化物A起反应;
据此,请填空:
(1)化合物F是__________ _;
(2)化合物I是_________ __;
(3)反应①的化学方程式是___________________________________________;
(4)反应④的化学方程式是___________________________________________;
(5)写出I的水溶液与A反应的方程式_____________________________________。
30.(13分)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
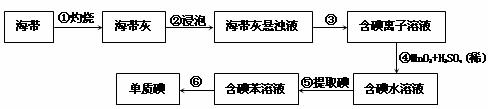
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。(3分)
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥管
(2)步骤③的实验操作名称是_________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是______________。(4分)
(3)步骤④反应的离子方程式是____________________________________。(2分)
(4)步骤⑤中,某学生选择用苯来提取碘的理由是_________________________。(2分)
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法______________
____________________________。(2分)
选做题:(以下三题31、32、33小题自选一题作答,多做不给分)
29.(13分)纯碱中常含有少量NaCl杂质,某实验小组用下图装置测定n g纯碱样品中Na2CO3的质量分数。
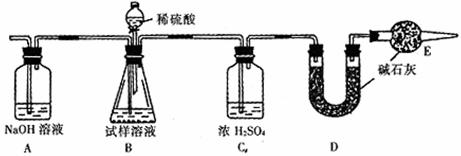
(1)测定实验的步骤为______________________。(填序号)(3分)
①称量盛有碱石灰的干燥管D的质量为m1 g;
②称量n g纯碱样品,将其放入锥形瓶内;
③按装置图组装仪器,并检查气密性;
④再次称量干燥管D的总质量为m2 g;
⑤从分液漏斗注入一定量的稀硫酸,直到B中不再产生气体为止。再缓缓鼓入空气一段时间。
(2)在用托盘天平称量样品时,如果天平的指针向右偏转,说明______________________
__________________________________________________________。(2分)
(3)装置E的作用是__________________________________,步骤⑤中“缓缓鼓入空气一段时间”的原因是_______________________________________________。(4分)
(4)A中NaOH溶液的作用________________________________。 (2分)
(5)该试样中纯碱的质量分数的计算式为_________________________________。(2分)
28.(17分)某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,设计如下方案:
|
|
操 作 |
结 论 |
|
甲 |
火柴梗 |
变黑者为浓硫酸 |
|
乙 |
加入金属铝片 |
产生刺激性气味者为浓硫酸 |
|
丙 |
分别加入到盛水的试管中 |
放热者为浓硫酸 |
|
丁 |
用玻璃棒蘸浓氨水靠近酸的瓶口 |
冒白烟者为浓硫酸 |
|
戊 |
加到CuSO4•5H2O晶体中 |
变白者为浓硫酸 |
(1)其中可行的是__________________(填序号)(3分)
(2)其中一个稍作改进就能成为可行的是__________,改进方法是__________________
________________________________________________________________。(4分)
(3)完全错误的是_______,因为___________________________________。(4分)
|
|
操 作 |
根据现象得出结论 |
|
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com