
14.下列离子方程式正确的是 ( )
A.氢氧化铁溶于过量的氢碘酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
B.氯化铝溶液中加入过量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
C.将氧化钠溶于水中:O2- + H2O = 2OH-
D.向过量的纯碱溶液中逐滴加入少量稀硝酸:CO32- + H+ = HCO3-
13.有关共价化合物的认识,一定正确的是 ( )
①具有较低的熔沸点 ②不一定是电解质
③固态时是分子晶体 ④液态时不导电
⑤其分子可能是极性分子 ⑥分子中不可能含非极性键
A.①③④ B.①②③④⑤⑥ C.②④⑤ D.⑤⑥
12.等体积、等物质的量浓度的稀硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能是 ( )
A.甲、乙中都是铝过量 B.甲中铝过量
C.甲中酸过量 D.乙中碱过量
11.下列物质不含有离子的是 ( )
A.氯化钠固体 B.铝粉 C.液态氯化氢 D.次氯酸钙
9.下列物质能用化合反应制取的是 ( )
①FeCl2 ② FeCl3 ③Fe(OH)3 ④Al2S3 ⑤NaOH
A.5种 B.4种 C.3种 D.2种
|
A.V(酸)= 102 V(碱) B.V(碱)= 102 V(酸)
C.V(酸)= 2 V(碱) D.V(碱)= 2 V(酸)
8.设NA 代表阿伏加德罗常数,下列说法中正确的是 ( )
①常温常压下,22.4 L N2所含有的原子数为2NA
②92 g NO2和92 g N2O4所含有的原子数均为6NA
③64 g铜被氧化时,一定失去2 NA电子
④ 常温常压下,100 mL 0.5 mol/L的乙酸溶液中,所含乙酸分子数小于0.05NA
⑤标准状况时,22.4 L二氯甲烷所含分子数为4NA ⑥ 标准状况时,1 mol氦气含有原子数为2NA
A.①② B.③④ C.②④ D.⑤⑥
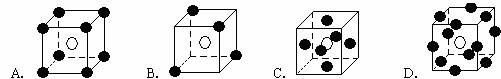
7.有下列离子晶体空间结构示意图,●为阳离子M,○为阴离子N,可以用以下哪一选项结构示意图表示化学式为MN2的晶体结构 ( )
6.在第四周期元素中,原子核外只有1个未成对的电子,这样的元素共有 ( )
A.3种 B.4种 C.5种 D.6种
5.下列操作 ①用稀NaOH溶液擦去沾在皮肤上的苯酚 ②用瓷坩埚灼烧烧碱固体 ③用酸式滴定管盛装酸性高锰酸钾溶液 ④加热蒸发皿时不用石棉网,其中正确的是 ( )
A.②③ B.③④ C.①④ D.都正确
4.不久前科学家合成了一种新型氧分子,它由4个氧原子构成,专家认为它液化后的能量比普通氧分子高得多。下列有关该分子的结论错误的是 ( )
A.它是氧分子的又一种同素异形体 B.分子中含有非极性共价键
C.1 mol该分子中含有24 mol电子 D.它将成为新型强力火箭推进氧化剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com