
8.某有机物的结构简式为: 关于该物质的叙述错误的是 ( )
A.一个分子中含有12个H原子
B.一氯代物有4种
C.能使酸性KMnO4溶液褪色
D.1mol该物质分别与足量H2、NaOH溶液反应,消耗H2、NaOH的物质的量均为3mol
7.根据 的结构,它不可能具有的性质是 ( )
A.与新制氢氧化铜反应 B.使溴的四氯化碳溶液褪色
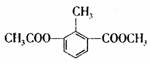 C.与乙醇在浓硫酸催化下发生酯化反应 D.与银氨溶液反应析出银
C.与乙醇在浓硫酸催化下发生酯化反应 D.与银氨溶液反应析出银
6.下列叙述正确的是 ( )
A.纯锌与稀硫酸反应时,加入少量CuSO4溶液,可使反应速率加快
B.甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:
CH3OH+6OH-+6e- === CO2+5H2O
C.在铁上镀铜时,金属铜作阴极
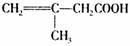 D.电解精炼铜时,电解质溶液中铜离子浓度不变
D.电解精炼铜时,电解质溶液中铜离子浓度不变
5.分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是 ( )
A.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物
B.HClO、浓H2SO4、HNO3均具有氧化性,都是氧化性酸
C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质
D.NaF、MgO、AlCl3均由活泼金属和活泼非金属化合而成,都是离子化合物
4.下列有关说法正确的是 ( )
A.制取蒸馏水是把杂质从水中蒸出
B.通过加热除去氯化铵固体中的碘单质
C.在做钠与水反应的实验时,为了安全起见,应在小烧杯上盖上表面皿或玻璃片
D.配制一定物质的量浓度的稀硫酸时,量取一定体积的浓硫酸注入小烧杯中,加水稀释冷却后转移到容量瓶中
3.判断反应过程的自发性的目的是 ( )
A.判断反应的方向
B.确定反应是否一定会发生
C.判断反应过程发生的速率
D.判断反应过程的热效应
1.2007年诺贝尔化学奖授予德国化学家Gerhard Ertl,以表彰他对固体表面化学研究过程中的重大发现。使CO、NOx等在铂表面发生化学反应转变成无毒气体,以减少汽车尾气中有毒气体的排放,正是此项研究的重要应用之一。下列有关说法不正确的是( )
A.CO在铂表面被氧化生成CO2,铂起催化作用
B.汽车尾气中NOx在铂表面发生还原反应的产物是N2
C.CO在铂表面可能和O2、NOx反应
D.NOx、CO、CO2均能与人体中的血红蛋白结合
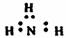 2.下列有关化学用语表达不正确的是 ( )
2.下列有关化学用语表达不正确的是 ( )
A.氨气分子的电子式: B.CO2分子的结构式:O=C=O

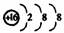
C.S2-的离子结构示意图: D.苯分子的比例模型:
22. (12分)已知可逆反应CO+H2O(g) CO2+H2,在一定条件下达到平衡状态。
(12分)已知可逆反应CO+H2O(g) CO2+H2,在一定条件下达到平衡状态。
(1)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,此时平衡常数K值为 ;水蒸气的转化率为 。
(2)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=6mol/L,则水蒸气的转化率为
。
(3)若T℃时,起始浓度c(CO)=amol/L,c(H2O)=bmol/L,平衡时H2的浓度c(H2) = cmol/L,则a、b、c之间的关系式是 ;
21.(12分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、Al3+、Ag+、Ba2+ |
|
阴离子 |
OH-、Cl-、CO2-3、NO-3、SO2-4 |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能有D反应产生沉淀。
试回答下列问题:
(1)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(2)写出E溶液与过量的B溶液反应的离子方程式:
。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-aKJ·mol-1。请写出B与C的稀溶液反应的热化学方程式 。
(4)在100mL0.1mol·L-1E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀的物质的量为 。
20.(14分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
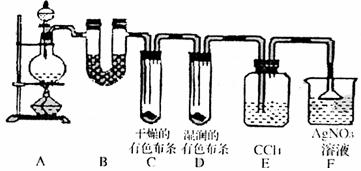
(1)下列方法中,可制得氯气的正确组合是 。
①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热
③次氯酸钠和浓盐酸混合 ④K2Cr2O7和浓盐酸混合
⑤KclO3和浓盐酸混合共热 ⑥KMnO4和浓盐酸混合
A.①②⑥ B.②④⑥ C.①④⑥ D.全部可以
(2)若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是
。
(3)①装置B的作用是 ,现象是 。
②装置C和D出现的不同现象说明的问题是
。
③装置E的作用是 。
④写出装置F中发生反应的离子方程式 。
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与 之间(填装置字母序号),装置中应放入 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com