
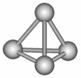
6.最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ热量。根据以上信息和数据,下列说法正确的是 ( )
A.N4属于一种新型的化合物
B.14N原子核内的中子数为7
C.N4沸点比P4(白磷)高
D.1molN4气体转变为N2吸收882kJ热量
5.下列反应的离子方程式正确的是 ( )
A.铜片插入氯化铁溶液中 Cu+Fe3+=Cu2++Fe2+
B.电解饱和食盐水 2Cl-+2H+ H2↑+C12↑
H2↑+C12↑
C.向溴化亚铁溶液中通入过量的氯气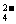 2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加足量Ba(OH)2溶液
NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O
4.化学反应前后肯定没有变化的是 ( )
①原子数目 ②分子数目 ③元素种类 ④物质的总质量 ⑤物质的种类
A.①④ B.①③⑤ C.①③④ D.①②③④
3.25℃时,PH和体积均相等的氨水和烧碱溶液中c(NH4+)与c(Na+)关系正确的是( )
A.c(NH4+)>c(Na+) B.c(NH4+)=c(Na+)
C.c(NH4+)<c(Na+) D.无法判断
2.有合成氨3H2+N2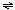 2NH3 现有A、B、C、D四只容器中,每个容器中有两种操作,两种操作分别达到平衡后,N2和NH3转化率之和不为1的是(起始体积相同): ( )
2NH3 现有A、B、C、D四只容器中,每个容器中有两种操作,两种操作分别达到平衡后,N2和NH3转化率之和不为1的是(起始体积相同): ( )
A.恒温恒容:操作一:加1mol N2和3mol H2; 操作二:加2molNH3
B.恒温恒压:操作一:加1mol N2和3mol H2; 操作二:加2molNH3
C.恒温恒容:操作一:加1mol N2和3mol H2; 操作二:加3molNH3
D.恒温恒压:操作一:加1mol N2和3mol H2; 操作二:加3molNH3
1.2005年美国《Science》上发表论文,宣布发现了一种Al的超原子结构,这种超原子(Al13)是以1个Al原子在中心,12个Al原子在表面形成的三角二十面体结构。这种超原子具有40个价电子时最稳定。请预测稳定的Al13所带的电荷为 ( )
A.-1 B.0 C.+2 D.+3
22. (12分)已知可逆反应CO+H2O(g) CO2+H2,在一定条件下达到平衡状态。
(12分)已知可逆反应CO+H2O(g) CO2+H2,在一定条件下达到平衡状态。
(1)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,此时平衡常数K值为 ;水蒸气的转化率为 。
(2)T℃时,若起始时:c(CO)=2mol/L,c(H2O)=6mol/L,则水蒸气的转化率为
。
(3)若T℃时,起始浓度c(CO)=amol/L,c(H2O)=bmol/L,平衡时H2的浓度c(H2) = cmol/L,则a、b、c之间的关系式是 ;
21.(12分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、Al3+、Ag+、Ba2+ |
|
阴离子 |
OH-、Cl-、CO2-3、NO-3、SO2-4 |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能有D反应产生沉淀。
试回答下列问题:
(1)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(2)写出E溶液与过量的B溶液反应的离子方程式:
。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-aKJ·mol-1。请写出B与C的稀溶液反应的热化学方程式 。
(4)在100mL0.1mol·L-1E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀的物质的量为 。
20.(14分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
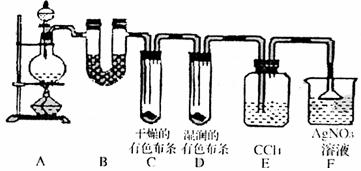
(1)下列方法中,可制得氯气的正确组合是 。
①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热
③次氯酸钠和浓盐酸混合 ④K2Cr2O7和浓盐酸混合
⑤KclO3和浓盐酸混合共热 ⑥KMnO4和浓盐酸混合
A.①②⑥ B.②④⑥ C.①④⑥ D.全部可以
(2)若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是
。
(3)①装置B的作用是 ,现象是 。
②装置C和D出现的不同现象说明的问题是
。
③装置E的作用是 。
④写出装置F中发生反应的离子方程式 。
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与 之间(填装置字母序号),装置中应放入 。
19.(8分)已知物质M由X、Y两种短周期元素组成,X原子的最外层电子数是最内层电子数的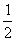 ,Y元素最高正价与它的负价代数和为6。M与其它物质的转化关系如下图所示(部分产物已略去):
,Y元素最高正价与它的负价代数和为6。M与其它物质的转化关系如下图所示(部分产物已略去):
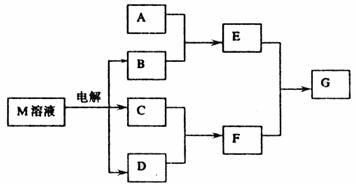
(1)若A是与X、Y同周期元素的一种常见金属单质,则A与B溶液反应的化学方程式是:
(2)若A是一种常见酸性氧化物,且可用于制造玻璃则E与F反应的离子方程式是:
(3)若A是一种常见的化肥,式量为79,且E与F反应生成G时有白烟产生,则G的电子式是
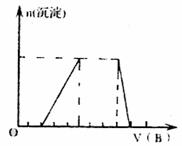
(4)若A是一种溶液,只可能含有H+、NH+4、Mg2+、Fe3+、Al3+、CO2-3、SO2-4中的某些离子,当向该溶液中加入B溶液时,发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com