
19.90℃时水的离子积Kw=3.8×10-13,该温度时纯水的pH ( )
A.小于7 B.等于7
C.大于7 D.无法确定
18.下面关于N2+3H2 2NH3;(△H<0)的平衡移动,(如下图)影响平衡移动的原因可能是: ( )
2NH3;(△H<0)的平衡移动,(如下图)影响平衡移动的原因可能是: ( )

A.升高温度,同时加压
B.减小压强,同时降温
C.增大反应物浓度,使用催化剂
D.增大反应物浓度,同时减少生成物浓度
17.下图里的曲线是在其它条件一定时,2NO+O2
 2NO2;(△H<0)
2NO2;(△H<0)
反应中NO的转化率与温度的关系曲线。图中标有a、b、c、d等四点,其中表示未达到平衡状态,且V(正)>V(逆)的点是( )

A.a点 B.b点 C.c点 D.d点
16.2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为: ( )
①2MoS2 + 7O2
 2MoO3 + 4SO2;
2MoO3 + 4SO2;
②MoO3 + 2NH3·H2O = (NH4)2MoO4 + H2O;
③(NH4)2MoO4 + 2HCl = H2MoO4↓+ 2NH4Cl;
④H2MoO4 = MoO3 + H2O;
⑤ 用还原剂将MoO3还原成金属钼。则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3不溶于氢氧化钠溶液
C.H2MoO4是一种强酸
D.利用H2、CO和铝分别还原等量的MoO3,消耗还原剂的物质的量之比为3:3:2
15.U常见化合价有+4和+6,硝酸铀酰[UO2(NO3)2]加热可发生如下分解,UO2(NO3)2 -- UxOY + NO2↑+ O2↑,在600K时,将气体产物收集于试管中并倒扣于中气体全部被吸收,水充满试管。则生成的铀的氧化物化学式是 ( )
A.UO2 B.UO3 C.2UO2·UO3 D.UO2·2UO3
11.准确量取25.00 mL的酸性KMnO4溶液,可选用的仪器 ( )
A.50 mL量筒 B.10 mL量筒
C.50 mL碱式滴定管 D.50 mL酸式滴定管
9.从植物花中提取一种有机物,可用简化式HIn表示,在水溶液中因存在下列电离平衡:HIn(溶液红色)  H+(溶液)+In-(溶液黄色),故可作酸碱指示剂。在该水溶液中加入下列物质,能使该指示剂显黄色的是 ( )
H+(溶液)+In-(溶液黄色),故可作酸碱指示剂。在该水溶液中加入下列物质,能使该指示剂显黄色的是 ( )
A.碳酸钠溶液 B.过氧化钠
C.氯化钠溶液 D. 盐酸
|
 H++OH–,向右移动且溶液呈酸性的是 ( )
H++OH–,向右移动且溶液呈酸性的是 ( )
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3溶液
C.向水中加入Na2CO3溶液 D.将水加热到100°C,使pH=6
8.下列图式正确的是 ( )
A.氟化氢的电子式: B.次氯酸的结构式: H-Cl-O
B.次氯酸的结构式: H-Cl-O
C.铝离子的结构示意图  D.氯化铯的晶体结构(晶胞)模型:
D.氯化铯的晶体结构(晶胞)模型: 
7.下列各组离子能在指定溶液中共存的是 ( )
①无色溶液中: 、
、 、
、 、
、 、
、 、
、
②使pH试纸变深蓝的溶液中: 、
、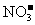 、
、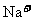 、
、 、
、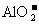 、
、
③水电离的 的溶液中:
的溶液中: 、
、 、
、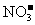 、
、 、
、
④加入Mg能放出 的溶液中:
的溶液中: 、
、 、
、 、
、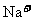 、
、
⑤使甲基橙变红的溶液中: 、
、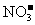 、
、 、
、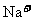 、
、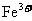
⑥pH=0的溶液中: 、
、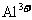 、
、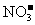 、
、 、
、 、
、
A.①③ B.②④⑤ C.①②⑤ D.③⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com