
8.莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是 ( )
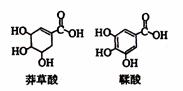
A.等物质的量的两种酸与足理金属钠反应产生氢气的量相同
B.两种酸遇三氯化铁溶液都显色
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.两种酸都不能与溴水反应
7.某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是 ( )
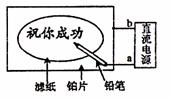
A.铅笔端作阳极,发生还原反应
B.a点是负极,b点是正极
C.铂片端作阴极,发生氧化反应
D.铅笔端有少量的氯气产生
6.判断下列有关化学基本概念的依据正确的是 ( )
A.强弱电解质:溶液的导电能力大小
B.共价化合物:是否含有共价键
C.氧化还原反应:元素化合价是否变化
D.金属晶体:晶体是否能够导电
5.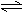 某温度下,某容积恒定的密闭容器中发生如下可逆反应:CO(g)+H2O(g) H2(g) +CO2(g);△H>0 当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是 ( )
某温度下,某容积恒定的密闭容器中发生如下可逆反应:CO(g)+H2O(g) H2(g) +CO2(g);△H>0 当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是 ( )
A.升高温度 B.加入催化剂
C.再加入2n mol CO2和2n mol H2 D.再加入n mol CO和n mol H2O
4.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.9kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g);△H=-192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g);△H=-192.9kJ·mol-1
下列说法正确的是 ( )

A.CH3OH的燃烧热为192.9 kJ·mol-1
B.反应①中的能量变化如右图变化
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+1/2 O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ·mol-1
3.下列符合化学实验“绿色化”的有 ( )
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水
②在铜和浓硝酸反应的实验中,将铜片改为可调节高度的铜丝
③将实验室的废酸液和废碱液中和后再排放
A.①② B.①③ C.②③ D.①②③
2.三氟化氮(NF3)是一种无色无味的气体,它是氨(NH3)和氟(F2)在一定条件下直接反应得到:4NH3+3F2=NF3+3NH4F,下列有关NF3的叙述正确的是 ( )
A.NF3是离子化合物 B.NF3中的N呈+3价
C.NF3的氧化性比F2强 D.NF3的还原性比NH3强
1.1828年,德国化学家乌勒(F·Wohler)冲破了生命力学说的束缚,在实验室里将无机物氰酸铵(NH4CNO)溶液蒸发,得到了有机物尿素[CO(NH2)2],他的这一功绩,恩格斯曾给予了很高的评价。下列说法中,不正确的是 ( )
A.氰酸铵属于铵盐 B.氰酸馆转变为尿素的过程为化学变化
C.有机物不一定要从生命体内获得 D.氰酸铵转变为尿素的过程为物理变化
31.(6分)把密度为1.68g / cm3的液态S2Cl2 10 mL 溶于石油醚(一种溶剂),得到100mL溶液,把它慢慢加入50 mL3.2mol/L的SO2 水溶液中,振荡使之充分反应,当加入的S2Cl2 溶液为64.3mL时,恰好反应完全。生成物用含0.32mol KOH的KOH溶液中和后,恰好完全转化为KCl 和一种二元含氧酸的钾盐晶体。试通过计算确定S2Cl2 与SO2 在溶液中反应的化学方程式。
30.(6分)恒温下,将a mol N2和b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3
H2(g)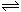 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,
计算a的值 。
(2)反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25% 。计算平衡时NH3的物质的量 。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同), n(始):n(平)= 。
(4)原混合气体中,a:b= 。
(5)达到平衡时,N2和H2的转化率之比,α(N2) :α(H2) = 。
(6)平衡混合气体中,n(N2):n(H2):n(NH3) =
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com