
7.同位素示踪法用于反应机理的研究,下列反应或转化中同位素示踪表示合理的是( )
A.NH4++2H2O NH3·2H2O+H+
NH3·2H2O+H+
B.2Na218O2+2H2O 4Na18OH+O2↑
4Na18OH+O2↑
C.2KMnO4+5H218O2+3H2SO4===K2SO4+2MnSO4+518O2↑+8H2O
D.K37C1O3+6HC1===K37C1+3C12↑+3H2O
6.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其他学式是NaA1(OH)2CO3。关于该物质的说法正确的是 ( )
A.该物质属于两性氢氧化物
B.该物质是A1(OH)3和Na2CO3的混合物
C.1 mol NaA1(OH)2CO3最多可消耗3molH+
D.该药剂不适合于胃溃疡患者服用
5.你认为下列物质不适合用作抑酸剂的是 ( )
A.碳酸钙 B.氢氧化铝 C.生石灰 D.小苏打
4.下列说法正确的是 ( )
①电解质溶液导电过程属于化学变化
②稀有气体不活泼的原因是它们原子的最外层都达到8电子稳定结构
③FeC12、CuS、NO都不能通过化合反应来制取
④SiO2是制造光导纤维的材料
A.②④ B.①④ C.①③④ D.②③
医疗上用的抑酸剂是为了减少胃内的盐酸而使用的药物。抑酸剂种类很多。请回答第5-6题
3.下列各组物质的分组正确的是 ( )
A.强电解质:NaOH、BaSO4、H2SO4 B.非电解质:SO2、F2、C2H5OH
C.碱性氧化物:MgO、CaO、Na2O2 D.同素异形体:H2O、D2O、T2O
2.现有四种物质:NaHCO3溶液、NaOH溶液、盐酸、铁粉。它们两两之间发生的反应最多有 ( )
A.3个 B.4个 C.5个 D.6个
1.观察是研究物质性质的一种基本方法。一同学将一小块金属钠露置于空气中,观察到下
列现象: ,下列说法正确的是 ( )
,下列说法正确的是 ( )
A.①发生了氧化还原反应 B.②变白色是因为生成了碳酸钠
C.③是碳酸钠吸收空气中的水蒸气形成了溶液 D.④只发生物理变化
22.(8分)据材料称:钠可在氮气中燃烧生成氮化钠,氮化钠与水反应的化学方程式是:
Na3N+4H2O=3NaOH+NH3·H2O。某学校化学研究学习小组,为了研究钠在空气中燃烧
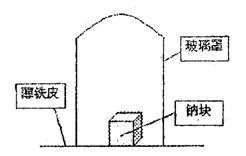
产物的成分,做了以下实验:取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠完全燃烧,将燃烧
产物投入水中,得到一种纯净气体0.224L(标准状态)和1.00L溶液,从中取出25.0mL溶液,和13.5mL 1.00mol·L-1HC1溶液刚好完全反应。求钠在空气中燃烧产物的成分及物质的量。
21.(8分)已知:①A、B、C为常见的单质,且单质B、C的元素同一主族,单质B、C的相对分子质量相等;
②F为正盐,B和I为气体且B无气味;
③沉淀H既可溶于盐酸又可溶于NaOH溶液,D、E的相对分子质量与H相同,向一定量的F溶液中逐渐加入固体粉末D或E,当D或E与F以物质的量之比3:1反应时,生成的沉淀H的量最多。其物质间的转化关系如下:
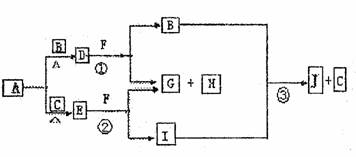
(1)写出D的电子式 ,E的化学式 。
(2)写出反应①的离子反应方程式 。
写出反应②的离子反应方程式 。
20.(10分)图1是氯碱工业中离子交换膜电解槽示意图,其中离子交换膜为“阳离子交换膜”,它有一特殊的性质--只允许阳离子通过,而阻止阴离子和气体通过。
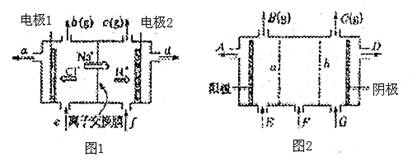
(1)电解后得到的氢氧化钠溶液从 口流出(填字母代号),b口排出的是 气体,电极1应连接电源的 极(填“正”或“负”);理论上讲,从f口加入纯水即可,但实际生产中,纯水要加入一定量的NaOH溶液,其原因是
和
。
(2)图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。请回答:a为 (填“阳”或“阴”)离子交换膜;从E口流进的物质的化学式(若为溶液,则写出溶质的化学式)
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com