
21.(9分)如图所示,将6molSO2和3molO2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g) 2SO3(g);△H<0。该反应达到平衡状态时,没得气体总物质的量为7.5mol。
2SO3(g);△H<0。该反应达到平衡状态时,没得气体总物质的量为7.5mol。
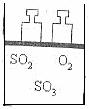
(1)在该平衡状态时n(SO3)= 。
(2)若起始时加入SO21.2mol,O20.6mol,和xmolSO3且达到平衡后各气体的体积分数与平衡状态相同,则x的取值范围为 。
(3)若反应开始时的v(逆)>v(正),达到上述平衡状态时,气体的总物质的量仍为7.5mol。则起始时n(SO3)的取值范围是 。
20.(8分)在相同容积的4个密闭容器中进行同一种可逆反应:2A(g)+B(g) 3C(g)+2D(g),起始时4个容器所盛A、B的量如下表所示
3C(g)+2D(g),起始时4个容器所盛A、B的量如下表所示
|
容器 |
甲 |
乙 |
丙 |
丁 |
|
A |
2mol |
1mol |
2mol |
1mol |
|
B |
1mol |
1mol |
2mol |
2mol |
在相同温度下,建立平衡时,4个容器中A的转化率由大到小的顺序为
B的转化率由小到大的顺序为 。
19.(9分)有甲乙两个容积相同的反应器,在甲容器中加入10克X和10克Y,乙容器中加入20克X和20克Y。分别密闭后加热到相同温度使之反应。
(1)若发生的反应是2X(g)+Y(g) 2Z(g)则反应速度是V甲 V乙,(大小、小于或等于,下同)达到平衡时X的转化率是甲 乙,X在平衡体系中体积百分含量是甲 乙。
2Z(g)则反应速度是V甲 V乙,(大小、小于或等于,下同)达到平衡时X的转化率是甲 乙,X在平衡体系中体积百分含量是甲 乙。
(2)若发生的反应是X(g)+Y(g) 2Z(g)则反应速度是V甲 V乙,达到平衡时X的转化率是甲 乙,X在平衡体系中体积百分含量是甲 乙。
2Z(g)则反应速度是V甲 V乙,达到平衡时X的转化率是甲 乙,X在平衡体系中体积百分含量是甲 乙。
(3)若发生的反应是X(g)+Y(s) 2Z(g)则反应速度是V甲 V乙,达到平衡时X的转化率是甲 乙,X在平衡体系中体积百分含量是甲 乙。
2Z(g)则反应速度是V甲 V乙,达到平衡时X的转化率是甲 乙,X在平衡体系中体积百分含量是甲 乙。
18.(10分)摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。下图是一个电化学过程的示意图。已知甲池的总反应式为:
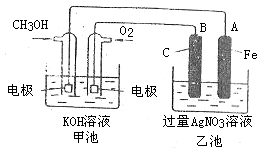
2CH3OH+3O2+4KOH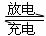 2K2CO3+6H2O
2K2CO3+6H2O
请填空:
(1)充电时:①原电池的负极与电源 极相连,②阳极的电极反应式为
。
(2)放电时:负极的电极反应式为: 。
(3)在此过程中若完全反应,乙池中A极的质量升高48g,则甲池中理论上消耗O2 L(标准状况下)。
(4)若在常温常压下,1gCH3OH燃烧在生成CO2和液态H2O时放热22.68KJ,表示该反应的热化学方程式为 。
17.(8分)把NaOH、MgC12、A1C13三种固体组成的混合物溶于足量水后,产生L16g白色沉淀,再向所得悬浊液中逐滴加入1.00mol/LHC1溶液,加入HC1溶液的体积与生成沉淀的关系如下图所示:试回答:
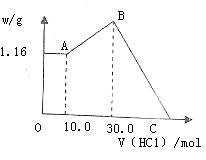
(1)A点的沉淀物的化学式为
理由 。
(2)写出A点到B点发生反应的离子方程式 。
(3)原混合物中MgC12物质的量是 ,A1C13物质的量是 ,NaOH物质的量是 。
(4)C点溶液的体积为 mL。
16.(8分)甲、乙、丙三位同学用规定的药品制备A1(OH)3,规定必用的药品如下:350g70%H2SO4溶液,NaOH固体240g,足量铝屑,水(不能用其它药品)甲、乙、丙用各自设计的方案制得A1(OH)3的质量分别是W1W2W3三种实验方案如下:
甲:铝→加 NaOH溶液→加H2SO4溶液→W1g(OH)3
乙:铝→加H2SO4溶液→加NaOH溶液→W2g(OH)3
 丙:铝→加H2SO4溶液
丙:铝→加H2SO4溶液
→W3gA1(OH)3
铝→加NaOH溶液
试回答:
(1)从充分利用原料、降低成本和提高产率等因素分析,实验方案最合理的是 。
(2)三位学生制得A1(OH)3、W1,W2,W3其质量依次是 、
、 。
15.(6分)
(1)将NaGHSO4溶液滴加到有酚酞试液的Ba(OH)2溶液中,当溶液颜色刚由红色变为无色时的离子方程式为 。
(2)向Ba(OH3)2溶液中滴入NaHSO4溶液,至沉淀完全,写出反应的离子方程式在上述溶液中继续滴入NaHSO4溶液,此时离子方程式是 。
14.将amolCu2S与cmol/LbL的硝酸恰好反应,生成硝酸铜、硫酸、一氧化氮、水。则参加反应的硝酸中,未被还原的硝酸的物质的量为 ( )
①4amol ②6amol ③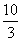 amol ④
amol ④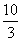 amol
amol
A.①② B.②③ C.①④ D.③④
卷Ⅱ
13.某单质能与足量浓硝酸反应放出NO2气体,若参加反应的单质和硝酸物质的量之比为1:a,则该元素在反应中所显示的化合价是 ( )
A.2a B.+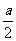 C.+
C.+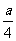 D.+a
D.+a
12.ALCO2气体通过足量Na2O2所得气体与bLNO混合时,可以cL气体(相同状况),以下表达式错误的是 ( )
A.若a<b,则c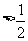 (a+b) B.若a<b,则c
(a+b) B.若a<b,则c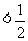 (a+b)
(a+b)
C.若a>b,则c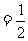 (a+b) D.若a=b,则c
(a+b) D.若a=b,则c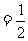 (a+b)
(a+b)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com