
25.500℃、20Mpa时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中
H2、N2和NH3物质的量变化如图所示,根据题意完成下列各题:
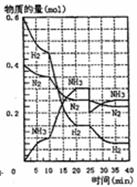
(1)反应达到平衡时,平衡常数表达式K= 此时增加N2的量,平衡常数将 (填“增大”“减小”或“不变”)
(2)500℃、20Mpa时,反应处于平衡状态的时间 。
(3)反应开始到第一次平衡时,N2的平均反应速率为 。
(4)据图判断,反应进行到10min至20min时曲线发生变化的原因是: 反应进行至25min时,曲线发生变化的原因是 。
24.在上海召开的第7届全球人类基因组大会上,我国科学家第一次提出可以用砒霜(As2O3)
来治疗早期性幼粒白血病。已知砒霜具有两性。
(1)完成并配平下列化学反应方程式:
As2O3+ Zn+ H2SO4→ AsH3+ ZnSO4+
(2)As2O3在上述反应中显示出来的性质是 ,H2SO4显示出来的性质是
(均填写编号)
①氧化性 ②还原性 ③酸性 ④碱性
(3)AsH3又称为胂。生产0.1mol胂,则转移电子的物质的量为 mol
(4)砷原子最外层电子排布式为 。在AsH3、PH3、H2S三种物质中,最不稳定的是
(5)砒霜在烧碱溶液中反应的离子方程式为
23.下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
|
a |
|
|
|
|
|
|
b |
|
|
|
|
d |
e |
f |
|
|
|
c |
|
|
g |
|
|
h |
|
(1)上述元素的单质中熔点最高的可能是 (填字母)。
(2)在一定条件下,a与e可形成一种极易溶于水的气态化合物,其电子式为
(3)现有另一种元素,其原子获得一个电子所释放的能量是上表中所列元素中最大的,则X是周期表中 族元素。
(4)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的 (填字母)元素组成,飞船中需要制造一种适合航天员生存的人工生态环境,还应该在氧气中充入一种稀释气体,该气体分子式为
。在运送飞船的火箭推进器中盛有分别由ae和af元素组成的两种液态化合物,它们的分子皆为18电子微粒,当它们混合反应时即产生e的单质和a2f。请写出该反应的化学方程式为 。
这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是 。
22.下列实验过程中产生的现象与对应的图形不相符合的是 ( )
A.NaHSO3粉末加入HNO3溶液中 B.H2S气体通入氯水中
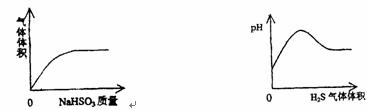
C.NaOH溶液滴入Ba(HCO3)2溶液中 D.CO2气体通入澄清石灰水中
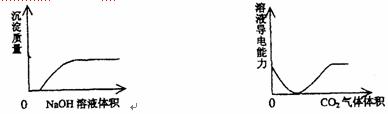
|
21.常温下把盐到的氨水等体积混合后,其溶液的pH值恰好等于7,则下列说法正确的是
( )
A.盐酸中C(H+)一定大于氨水中C(OH-)
B.盐酸的物质的量浓度一定小于氨水的物质的量浓度
C.反应后生成的盐溶液没有发生水解
D.盐酸中氯化氢的物质的量等于氨水中氨的物质的量
20.下列溶液中各微粒的浓度关系不正确的是 ( )
A.0.1mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.1L 0.1mol·L-1 CuSO4·(NH4)2SO4·6H2O的溶液中:
c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-)
C.0.1mol·L-1 NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
D.等体积、等物体的量浓度的NaX和弱酸HX混合后的溶液中:
c(Na+)>c(HX)>c(X-)>c(H+)>(OH-)
|
|
C3N3(OH)3 3HNCO;8HNCO+6NO2 7N2+8CO2+4H2O
下列说法正确的是 ( )
A.C3N3(OH)3与HNCO为同一物质
B.HNCO是一种很强的氧化剂
C.1mol NO2在反应中转移的电子为4mol
D.反应中NO2是还原剂
19.为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂。已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如右图所示。下列叙述中正确的是 ( )
A.该物质可以视为酚类
B.在浓硫酸作用下,分子内消去一个水分子,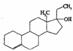 产物有二种同分异构体
产物有二种同分异构体
C.能使溴的四氯化碳溶液褪色
D.该物质分子中的所有碳原子均共面
17.在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)2、AgNO3各0.01mol的溶液加入0.01mol铁粉,充分搅拌后发生的变化是 ( )
A.铁溶解,但没有其他金属析出
B.铁溶解,只析出0.01mol银
C.铁溶解,析出0.01mol银和0.005mol铜
D.铁溶解,只析出0.01mol铜
16.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是 ( )
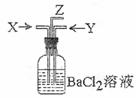
A.在Z导管口有红棕色气体出现
B.在Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.洗气瓶中产生的沉淀是碳酸钡
15.工业生产苯乙烯同是利用乙苯的脱氢反应:
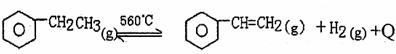
针对上述反应,在其它条件不变时,下列说法正确的是 ( )
A.加入适当催化剂,可以提高乙苯的转化率
B.在保持体只一定的条件下,充入较多的乙苯,可以提高乙本的转化率
C.在加入乙苯至达到平衡过程中,混合气体的平均相对分子质量在不断增大
D.仅从平衡移动的角度分析,工业生产苯乙稀选择恒压条件优于恒容条件
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com