
14.已知可逆反应aA+bB 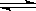 cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是(
)
cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是(
)
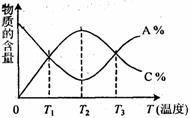
A.该反应在T1.T3温度时达到过化学平衡
B.该反应在T2温度时达到化学平衡
C.升高温度,平衡会向正反应方向移动
D.该反应的正反应是吸热反应
13.25℃时,水的电离达到平衡:H2O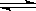 H++OH-;ΔH>0,下列叙述正确的是(
)
H++OH-;ΔH>0,下列叙述正确的是(
)
A.向水中加入稀氨水,平衡逆向移动,c(OH―)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
12.用已知浓度的盐酸测定未知浓度的NaOH溶液的物质的量浓度,进行酸碱中和滴定时,将碱滴入酸中,下列操作都会使测定结果偏低的是(锥形瓶中溶液用滴定管量取)( )
A.碱式滴定管未用待测碱液润洗 B.酸式滴定管未用标准盐酸润洗
C.滴定过程中不慎锥形瓶中有液体溅出 D.滴定前仰视读数,滴定后读数正确
11.表示0.1mol·L-1NaHCO3溶液有关微粒浓度的关系正确的 ( )
A.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)
D.c(OH-)=c(H+)+c(H2CO3)+c(HCO3-)
10.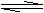 在一定温度下,可逆反应:2HI(g)
H2(g)+I2(g),△H>0,已知平衡状态改变某一
在一定温度下,可逆反应:2HI(g)
H2(g)+I2(g),△H>0,已知平衡状态改变某一
|
A.改变的条件可能是在恒容条件下,充入HI气体
B.改变的条件可能是在恒压条件下,充入HI气体
C.化学平衡一定向正反应方向移动
D.正反应速率增大,逆反应速度一定减小
9.下列物质的提纯或离子检验的方法正确的是 ( )
A.用渗析的方法精制氢氧化铁胶体
B.以精铜为阳极,粗铜为阴极,CuSO4溶液为电解液精炼铜
C.除去KCl溶液中的少量MgCl2,加入过量KOH溶液,然后过滤即可
D.加入澄清的石灰水,能产生白色沉淀,则原溶液中一定含有CO32-
8.下列叙述正确的是 ( )
①锌跟稀硫酸反应制H2,加入少量硫酸铜溶液能加快反应速率;
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀;
③电镀时,应把镀件置于电解槽的阴极;
④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解;
⑤钢铁表面常易腐蚀生成Fe2O3·nH2O
A.全部 B.①③④⑤ C.①③⑤ D.②④
7.在含有Cu(NO3)2.Zn(NO3)2 Fe(NO3)3.AgNO3各0.1mol的混合溶液中加入0.1mol Fe粉,
充分搅拌后铁溶解,溶液中不存在Fe3+离子,同时析出0.1molAg。则下列结论中不正确的是 ( )
A.溶液中Cu2+与Fe2+的物质的量之比为1:2
B.氧化性:Ag+>Cu2+>Fe3+>Zn2+
C.Fe3+的氧化性大于Cu2+
D.1molFe可还原2molFe3+
6.下列离子方程式正确的是 ( )
A.过量的NaHSO4和Ba(OH)2溶液反应:H+ + SO42- + Ba2+ + OH- == BaSO4↓ +2H2O
B.NH4HCO3和过量NaOH溶液相混合:HCO3- + OH- == CO32- + H2O
C.NaHSO4溶液中滴加NaHCO3溶液:H+ + HCO3- == H2O + CO2↑
D.用氨水吸收少量的SO2:NH3 + H2O + SO2 == NH4+ + HSO3-
5.用NA表示阿伏加德罗常数的数值,下列说法正确的是 ( )
A.在标准状况下,VL水含有的氧原子个数为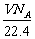
B.1/18 mol的1H35Cl分子所含中子数为NA
C.1mol FeCl3与水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
D.常温时1 L 1mol/L的醋酸溶液中,所含醋酸分子数为NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com