
7.对下列各种溶液中所含离子的判断合理的是
A.向无色溶液中加氯水变橙色,溶液中可能含:SO42-,Br-,OH-,Ba2+
B.在c(H+)=10-14mol/L的溶液中可能含:Na+,AlO2-,CO32-,SO32-
C.在常温下加入铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3-
D.使紫色石蕊试液变红色的溶液中可能含:K+,Na+,Ca2+,HCO3-
6.对于发生反应M+N=W+V的化学反应中,下列说法正确的是
A、若M、W为单质,N、V为化合物,该反应不一定是置换反应
B、W、V为盐和水,该反应不一定是中和反应
C、若M、N为m克,则反应后W、V的质量和一定是m克
D、反应物M,N的质量比一定等于W,V的质量比
5.镁、铝、铜三种金属粉末混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤液中存在的离子有
A.[Al(OH)4]- B.Cu2+ C.Al3+ D.Mg2+
4.实验室有一瓶久置的白色粉末,经元素分析证明它由钾、硫、氧三种元素组成,钾和硫的质量比39:16,下列结论正确的是
A、根据元素分析的结果推测该粉末是纯净物
B、将粉末溶于水,加入氯化钡,观察有白色的沉淀生成,证明原来的粉末是硫酸钾
C、将粉末溶于水,加入氯化钡和盐酸,观察到有白色沉淀和气泡产生,则原粉末可能是硫酸钾和亚硫酸钾的混合物
D、将粉末加入盐酸,产生气泡,证明原粉末一定是亚硫酸钾
3.下列关于胶体说法正确的是
A、胶体都是液体
B、具有丁达尔效应是胶体的本质特征
C、胶体具有和其它分散系不同的性质,原因在于其分散质微粒大小与其它分散系不同
D、向溶胶中加入任何一种溶液,都可使溶胶发生聚沉。
2.氢叠氮酸(HN3)与醋酸性质相似,其盐稳定, 但是在受到撞击时发生爆炸生成氮气。有关氢叠氮酸及其盐的叙述不正确的是:
A、NaN3可用于汽车防撞保护囊 B、NaN3的水溶液呈碱性
C、NaN3 的固体属于离子晶体 D、HN3分子中各原子都满足于8个电子稳定结构
1.下列有关叙述正确的是:
A、铜可导电,所以铜是电解质
B、MgCl2在熔融状态下可导电,它是电解质
C、HCl、H2SO4液态时都不导电,都是非电解质
D、能导电的单质一定是金属
33.为了测定K2CO3和NaHCO3混合物的组成,某学生每次称取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的Ba(OH)2溶液,每次实验均充分反应,实验结果记录如下表:
|
实验次数 |
混合物的质量/g |
所加Ba(OH)2溶液的体积/L |
测得沉淀的质量/g |
|
1 |
0.858 |
0.5 |
1.379 |
|
2 |
1.716 |
0.5 |
|
|
3 |
2.574 |
0.5 |
4.137 |
|
4 |
3.432 |
0.5 |
5.516 |
|
5 |
4.290 |
0.5 |
5.516 |
|
6 |
5.148 |
0.5 |
5.516 |
请回答下列问题:
(1)第二次实验中产生沉淀的质量是 g;
(2)求所用Ba(OH)2的溶液的物质的量浓度?
计算过程:
(3)求混合物中K2CO3和NaHCO3的物质的量之比?
计算过程:
(4)在25℃时,取下第3组实验所得溶液体积的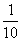 ,加水配成500mL溶液,求此溶液PH?
,加水配成500mL溶液,求此溶液PH?
计算过程:
32.6.4gCu与过量硝酸(amol/L,30mL)充分反应。硝酸的还原产物只有NO2、NO。反应后溶液中含H+为0.1mol.
(1)此时溶液中所含NO-3为 mol。
(2)求生成的气体中NO2和NO的物质的量各为多少(用含有a的式子表示)?
32.已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性:Mg和Na的化学性质也具有一定相似性。
用如图所示装置进行Mg与SO2反应的实验。
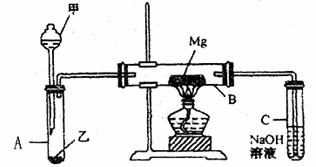
(1)选择制取SO2的合适试剂
①10%的H2SO4溶液②27%的H2SO4溶液③Na2SO3固体④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式
装置C中NaOH溶液的作用是
(3)你认为该装置是否有不足之处? 。如果有,请说明 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com