
24.(12分)下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。
|
b |
|
|
|||||||||||||||
|
|
|
|
|
h |
|
j |
|
|
|||||||||
|
a |
c |
|
f |
g |
|
i |
k |
l |
|||||||||
|
|
|
|
|
|
|
|
e |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
d |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)写出表中所有代表金属元素的元素符号 ;
(2)表中各元素的单质中,属于分子晶体的有 (写分子式)。
(3)写出h与i元素组成的分子的电子式 ,该分子属于
(极性、非极性)分子。
(4)写出满足以下要求的3个置换反应的化学方程式:①从表内短周期元素中挑选出6种单质,②6种单质分属6个不同的主族。 ;
; 。
23.(5分)某化学反应的反应物和产物如下:
KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化产物是
(2)如果该反应方程式中I2和KIO3的化学计量数都是5;①KMnO4的化学计量数是 ;②在下面的化学式上标出电子转移的方向和数目
KMnO4 + KI + H2SO4 →
22.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH+、Cl─、Mg2+、Ba2+、SO42─、CO32─,现取三份100mL溶液进行如下实验:⑴ 第一份加入AgNO3(aq)有沉淀产生;⑵ 第二份加足量NaOH(aq)加热后,收集到气体0.04mol;⑶ 第三份加足量BaCl2(aq)后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是: ( )
A.K+一定存在 B.100mL溶液中含有0.01mol CO32─
C.Cl─ 一定存在 D.Ba2+一定不存在,Mg2+可能存在
|
21.欲使NaHCO3稀溶液中H+、CO32─、HCO3─的浓度均减少,可加入或通入: ( )
A.NaOH固体 B.澄清石灰水 C.浓盐酸 D.CO2
20.在100 mL FeI2溶液中缓缓通人标准状况下的氯气3.36 L,反应完全后,溶液中有一半的Fe2+被氧化生成Fe3+,则原来FeI2溶液的物质的量浓度为: ( )
A.l.0 mol·L─1 B.1.2 mol·L─1 C.1.5 mol·L─1 D.0.6 mol·L─1
19.下列各组离了在溶液中能大量共存,且加入过量NaOH溶液或过量稀盐酸均能得到澄清溶液的是: ( )
A.Fe2+、K+、SO42─、Cl─ B.Ca2+、Mg2+、HCO3─、NO3─
C.Al3+、Na+、SO42─、NO3─ D.K+、Na+、SiO32─、AlO2─
18.不能通过化合反应制取的是: ( )
A.FeCl2 B.NaHCO3 C.H2SiO3 D.Fe(OH)3
17.将SO2气体通入BaCl2溶液至饱和,未见有沉淀生成,
继续通入另一种气体仍无沉淀产生。则通入的该气体可能是: ( )
A.CO2 B.NH3 C.NO2 D.Cl2
16.如图所示甲、乙两个装置中,分别挤压胶头滴管向广口瓶中加入液体,两装置中的气球都明显地胀大(忽略液体体积对气球的影响)。则相应的胶头滴管和广口瓶中所用试剂可能是: ( )
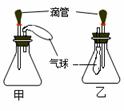
A.甲:NaOH溶液和CO2,乙:H2O2和MnO2
B.甲:CaCl2和Na2CO3溶液;乙:NaOH 溶液和Cl2
C.甲:浓硝酸和铝片,乙:溴水和二氧化硫
D,甲:浓硫酸和蔗糖,乙:水和氯化氢
15.用类推的方法可能会得出错误结论,因此类推出的结论要经过实践的检验才能确定其正确与否。下列类推结论中正确的是: ( )
A.工业上电解熔融MgCl2制取金属镁,工业上也用电解熔融AlCl3的方法制取金属铝
B.Mg失火不能用CO2灭火,Na失火也不能用CO2灭火
C.Al与S直接化合可以得到A12S3,Fe与S直接化合也可以得到Fe2S3
D.Fe3O4可以写成FeO·Fe2O3,Pb3O4也可写成PbO·Pb2O3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com