
5. 已知:C(s) + CO2(g)
2CO(g);△H>0。该反应达以平衡后,下列条件有利于平衡向逆反应方向移动的是 ( )
已知:C(s) + CO2(g)
2CO(g);△H>0。该反应达以平衡后,下列条件有利于平衡向逆反应方向移动的是 ( )
A.升高温度和减小压强 B.降低温度和减小压强
C.降低温度和增大压强 D.升高温度和增大压强
4.有关晶体的下列说法中正确的是 ( )
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
3.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是
( )
A.植物油不能使溴的四氯化碳溶液褪色
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应
D.蛋白质溶液遇到硫酸铜后产生的沉淀能重新溶于水
2.下列叙述错误的是 ( )
A.13C和14C互为同位素
B.白磷和红磷互为同素异形体
C.乙二醇和丙三醇互为同系物
D.新戊烷和异戊烷互为同分异构体
1.下列家庭实验中不涉及化学变化的是 ( )
A.用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐
B.用少量食醋除去水壶中的水垢
C.用糯米、酒曲和水制甜酒酿
D.用小苏打与酒石酸混合制发酵粉蒸馒头
34.用高锰酸钾氧化密度为1.19g/cm3,质量分数为36.5%的盐酸。反应如下:
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
求:(1)被15.8gKMnO4氧化的盐酸的体积(3分)
(2)生成Cl2在标况下的体积(3分)
(3)反应中转移的电子总数(2分)
33.(9分)在实验室中用二氧化锰和浓盐酸反应制备干燥的氯气,装置图如下:
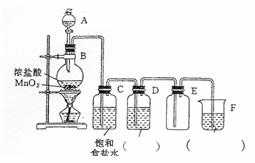
(1)写出B中发生反应的化学方程式 。
(2)C中饱和食盐水的作用是 。
(3)D中所盛试剂是 ,作用是 。
(4)E用的是向 排空气法收集气体。
(5)F中盛放的试剂是 ,反应的离子方程式为 。
32.(8分)现用质量分数为98%,密度为1.84g/cm3的浓硫酸来配制500ml 0.2mol/L的稀硫酸,可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④量筒 ⑤容量瓶 ⑥托盘天平⑦药匙
(1)上述仪器中,配制过程中用不到的有 。
(2)计算所需浓硫酸的体积为 。现有①10ml ②50ml ③100ml三种规格的量筒,最好选用 。(填代号)
(3)在配制过程中,下列操作可引起所配溶液浓度偏高的有 。(填代号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到定量瓶中。
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒
⑤定容量,俯视刻度线
31.(2分)已知反应:2FeCl3+2KI=2FeCl2+2KCl+I2
2FeCl2+Cl2=2FeCl3
I2+SO2+2H2O=H2SO4+2HI
I-、Fe2+、Cl-和SO2的还原能力由强到弱的顺序为 。
30.(2分)已知反应:5HClO3+6P+9H2O=5HCl+6H3PO4,用双线桥表示出此反应中电子转移的方向和数目 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com