
25.(6分)有机化合物A的分子式是C13和H20O8(相对分子质量为304),1mol A在酸性条件下水解得到4 mol CH3COOH和1mol B。B分子结构中每一个连有羟基的碳原子上还连有两个氢原子。请回答下列问题:
(1)A与B的相对分子质量之差是 。
(2)B的结构简式是 。
(3)B的不能发生的反应是 。(填写序号)
①氧化反应 ②取代反应 ③消去反应 ④加聚反应
24.(9分)现有含CaO杂质的CaC2试样。某研究性学习小组的同学拟用以下两种方案测定CaC2试样的纯度。请填写下列空白:
(1)第一种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度。
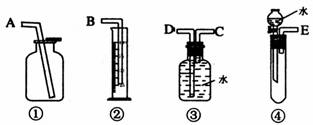
①选用装置的连接顺序应是(填各接口的字母): 。
②为得到平稳的气流,可用 代替水。
③若实验时称取的试样为1.40g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为 。
(2)第二种方案:称取一定质量的试样,操作流程如下:
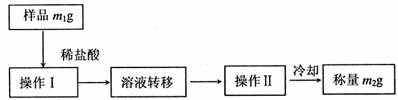
①操作Ⅰ、Ⅱ的名称分别是 、 。
②某学生在计算过程中设CaC2的物质的量为x mol,CaO的物质的量为y mol,请你列出一个关于x、y、m1、m2的方程组 。
23.(8分)(1)如图所示,图1、图2为中学化学常的气体发生装置。
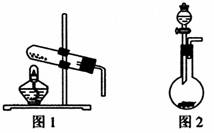
①若用图1装置制备氨气,写出化学方程式 。
②若用图2装置制备氨气,写出所需试剂名称 。
③若用图2装置制备氧气,写出化学方程式 。
(2)利用图3装置,在实验室中可制备下列哪些气体 (填序号)。
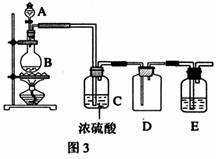
①C2H4 ②NO2
③NO ④Cl2
⑤CO2
22.(12分)短周期元素A、B、C、D的原子序数依次增大。
①C的最外层电子数比最内层电子数少一个;
②A、B形成的化合物X与B的最高价氧化物对应的水化物Y,发生化合反应生成Z;
③电解C、D 形成的化合物的水溶液,两极均放出气体且相同条件下气体体积相等。
试回答:
(1)B为 ,D为 (填元素符号),X的电子式为 。
(2)X和Y生成Z的离子方程式为 ;Z的水溶液呈现 (填“酸性”、“碱性”或“中性”),用离子方程式说明原因
。
(3)当电解C、D形成的化合物(足量)的水溶液500mL时,两极共产生气体1120mL(标况),则溶液的pH= (假设溶液体积不变,温度为常温)
(4)A单质和B单在一定条件下发生反应,当起始加入nA: nB=1:1时,A单质的转化率
B单质的转化率(填“大于”、“小于”或“等于”)。
21.(4分)已知X和Y均是短周期元素中的同主族元素的单质,W、V是化合物,它们有如下变化关系:X+W→Y+V
试写出符合题意,且满足下列关系的化学方程式:
(1)W是水 ;
(2)V是水 。
20.某芳香族有机物的分子式为C8H6O2,它的分子(除苯环外不含其他环)中不可能有( )
A.两个羟基 B.醛基 C.两个醛基 D.羧基
|
19.下列除去杂质的方法正确的是 ( )
①除去甲烷中少量的乙烯:将混合气体通过酸性高锰酸钾;
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤;
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A.①② B.②④ C.③④ D.②③
18.下列有关工业生产的叙述正确的是 ( )
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
C.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
17.在25℃时,将pH=3的HCl溶液和pH=11的氨水等体积混合后,溶液显碱性,下列关系式中正确的是 ( )
A.c(Cl-)=c(NH4+)+c(NH3) B.c(OH-)=c(H+)+c(NH4+)
C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
16.R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法一定正确的是(m、n均为正整数) ( )
A.若HnXOm为强酸,则Y是活泼非金属元素
B.若R(OH)m为强碱,则W(OH)n也为强碱
C.若Y的最低化合价为-2,则Z的最高正化合价为+6
D.若X的最高正化合价为+5,则五种元素都是非金属元素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com