
18.某溶液中大量存在以下五种离子:NO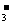 、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO
、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO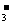 )︰n(SO42-)︰n(Fe3+)︰n(H
)︰n(SO42-)︰n(Fe3+)︰n(H )︰n(M)=2︰3︰1︰3︰1,则M可能是 ( )
)︰n(M)=2︰3︰1︰3︰1,则M可能是 ( )
A.Fe2+ B.Mg2+ C.Cl D.Ba2+
D.Ba2+
17.下列有关热化学方程式的叙述中,正确的是 ( )
A.含20.0 g NaOH 的稀溶液与稀盐酸完全中和,放出28.7 kg的热量,则表示该反应中和热的热化学方程式为:HCl(aq)+NaOH(aq)= H2O(l)+ NaCl(aq);ΔH=-57.4 kJ· mol-1
B.由4P(s,红磷)= P4(s,白磷);ΔH >0 可知,白磷的热稳定性比红磷大
C.已知2H2(g)+O2(g)=2H2O(g);ΔH=-483.6 kJ·mol-1 ,则H2 的燃烧热为241.8 kJ·mol-1
D.已知2C(g)+ 2O2(g)=2CO(g);△H1
2C(s)+ O2(g)=2CO(g);△H2 ,则△H1 <△H2
16.下列离子方程式中正确的是 ( )
A.将少量的Ba(OH)2溶液加入到NH4HSO4溶液中:
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH- == NH3↑+H2O
C.苯酚钠溶液中通入少量CO2 : -O-+CO2+H2O→
-O-+CO2+H2O→ -OH+HCO3-
-OH+HCO3-
D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2→2Fe3++Br2+4Cl-
15.下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是
( )
A.Na+、K+、AlO2-、Cl- B.K+、Na +、HCO3-、SO42-
C.Na+、K+、S2-、SO32- D.Ba2+、Na+、I-、NO3-
14.下列说法不正确的是 ( )
A.活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同
B.同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等
C.将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成
D.将足量Cl2通入NaBr、NaI的混合溶液中,反应后将溶液蒸干并充分灼烧,剩余的固体物质成分为NaCl
13.下列说法不正确的是 ( )
A.28g乙烯与28g丙烯中均含有6NA对共用电子对
B.1 mol H2O2在MnO2作催化剂的条件下完全分解,转移电子数为2NA
C.标准状况下,3.5g 35Cl2所含中子数为1.8NA
D.常温常压下,22g氧气和26g臭氧混合后,混合气体所含氧原子总数为3NA
12.二氧化硫的催化氧化是放热反应。下列关于接触法制硫酸的叙述中正确的是 ( )
A.为防止催化剂中毒,炉气在进入接触室之前需要净化
B.为提高SO2的转化率,接触室内反应温度选定在400℃~500℃
C.为防止污染大气,从吸收塔出来的尾气常用NaOH溶液吸收
D.为提高SO3的吸收效率,用稀硫酸代替水吸收SO3
11.下列物质存放方法正确的是 ( )
A.药品柜的同一层不可同时存放浓硝酸和浓氨水
B.少量的钠保存在无水乙醇中
C.少量白磷保存在二硫化碳中
D.硅酸钠溶液保存在有玻璃塞的试剂瓶中
9.进行下列实验肯定不能获得成功的是 ( )
A.用pH试纸鉴别浓硫酸与浓硝酸
B.用硝酸银溶液区分二氧化氮和溴蒸气
C.用酸性高锰酸钾溶液除去二氧化碳中混有的少量二氧化硫
D.用溴水除去苯中溶有的少量苯酚
|
8.下列各物质相互反应时,水既不作氧化剂又不作还原剂,但属于氧化还原反应的是( )
①F2与H2O ②Na2O2和H2O ③NO2与H2O ④Cl2+H2O ⑤K与FeCl3溶液
⑥P2O5与H2O
A.①②③ B.②③④ C.②④⑤ D.④⑤⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com