
12.下列反应的离子方程式书写正确的是 ( )
A.过量的SO2通入NaOH溶液中:
SO2+2OH-= SO2-3+H2O
B.NaHCO3溶液中加入过量的Ba(OH)2溶液:
HCO-3+Ba2++OH-=BaCO3↓+H2O
C.硫酸亚铁溶液与稀硫酸、双氧水混合:
2Fe2++H2O2+2H+=2Fe3++2H2O
D.氯化铝溶液加入过量的氨水:
Al3++4OH-=AlO-2+2H2O
11.将2mol NaHCO3和一定量的Na2O2固体混合,在加热条件下使其充分反应,在150℃下所得气体仅含2种组分,反应后固体的物质的量n的取值范围是 ( )
A.n = 1 B.1<n<2 C.2≤n<4 D.n≥4
9.下列每组各有三对物质,它们都能用分液漏斗分离的是 ( )
①乙酸乙酯和水,酒精和水,苯酚和水
②二溴乙烷和水,溴苯和水,硝基苯和水
③甘油和水,乙醛和水,乙酸和乙醇
④油酸和水,甲苯和水,乙烷和水
A.①② B.②④ C.③④ D.①②④
|
8.一定条件下,磺单质与砹单质以等物质的量进行反应,可得AtI。它与Zn、NH3都能发生反应,化学方程式分别如下2AtI+2Zn == ZnI2+ZnAt2 AtI + 2NH3(I) ===NH4I+NH2At则下列叙述正确的是 ( )
A.ZnI2既是氧化产物,又是还原产物
B.ZnAt2既是氧化产物,又是还原产物
C.AtI与液氨反应,AtI既是氧化剂又是还原剂
D.AtI与液氨反应,属于氧化还原反应
7.常温下,下列溶液中一定能大量共存的离子组是 ( )
A.含有大量S2-的溶液:ClO-、Na+、Cl-、CO2-3
B.无色澄清溶液:MnO-4、SO2-4、K+、Fe3+
C.能使pH试纸变红的溶液:NH+4、Na+、SO2-4、Fe3+
D.水电离产生的c(H+) = 1×10-12mol/L的溶液:HCO-3、NH+4、Cl-、Ca2+
6.一定量的锎(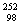 Cf)是医学上常用作治疗恶性肿瘤的中子源,1mg(
Cf)是医学上常用作治疗恶性肿瘤的中子源,1mg(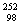 Cf)每秒约放出2.34×199个中子。下列有关锎的说法错误的是 ( )
Cf)每秒约放出2.34×199个中子。下列有关锎的说法错误的是 ( )
A.(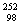 Cf)原子中,中子数为154 B.(
Cf)原子中,中子数为154 B.(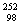 Cf)原子中,质子数为98
Cf)原子中,质子数为98
C.(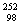 Cf)原子中,电子数为98 D.锎元素的相对原子质量为252
Cf)原子中,电子数为98 D.锎元素的相对原子质量为252
5.下列有关物质结构的叙述,不正确的是 ( )
A.含有非极性键的分子不一定是非极性分子
B.分子晶体的熔沸点与共价键的强弱没有直接的关系
C.共价化合物中一定有极性共价键,离子化合物中可能有极性共价键
D.含离子键的化合物一定是离子化合物,熔融状态时能导电的晶体一定是离子晶体
4.实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别是 ( )
A.1000mL,212g B.950mL,201.4g
C.任意规格,572g D.500mL,106g
3.阿伏加德罗常数约为6.02×1023mol-1,下列说法正确的是 ( )
A.4.5g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023
B.7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA
C.17gOH-含有9×6.02×1023个电子
D.标准状况下,11.2LSO3中含有氧原子数目为1.5×6.02×1023
2.将钠投入到下列溶液中,反应的剧烈程度由强到弱的是 ( )
①水 ②NaOH溶液 ③0.1mol/L盐酸 ④0.1mol/L硫酸铁溶液
A.④③②① B.④③①② C.③④①② D.①③④②
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com