
6.下列物质加入稀盐酸,都能生成使澄清石灰水变浑浊的气体的是 ( )
①大理石 ②漂白精 ③鸡蛋壳 ④硫代硫酸钠 ⑤二氧化硅
A.①②③ B.①③④ C.①③⑤ D.②④⑤
5.下列各组物质的熔点变化规律,与它们的化学键无关的是 ( )
A.F2、Cl2、Br2、I2的熔点依次升高
B.H、Na、K、Rb的熔点依次降低
C.NaF、NaCl、NaBr、NaI的熔点依次降低
D.晶体硅、碳化硅、金刚石的熔点依次升高
4.下列实验事故处理方法不得当的是 ( )
A.苯酚不慎沾到手上,应立即用酒精清洗
B.酒精洒在桌面上引起失火,可以用水来浇灭
C.皮肤感染后,可以用稀双氧水进行清洗
D.浓盐酸沾到手上,立刻用大量水进行清洗
3.下列各组物质发生化学反应时,由于反应物的量不同生成不同产物的是 ( )
①CO2与NaOH溶液 ②P与Cl2
③AgNO3溶液与氨水 ④C与O2
⑤AlCl3溶液与氨水 ⑥C2H2与Cl2
⑦NaHCO3溶液与盐酸
A.除⑦外 B.除②⑥外 C.除③⑦外 D.除⑤⑦外
2.最近意大利罗马大学的Fulvio Cacace等科学家获得了具有理论研究意义的分子N4,其结构与白磷相似,一个N4分子中的四个氮原子位于正四面体的四个顶点,如下图所示,下列关于N4的说法中正确的是 ( )

A.N4是一种新型的化合物
B.N4与N2互为同素异形体
C.N4稳定性比白磷差
D.N4属于原子晶体
1.下列物质均具有漂白性,其中有一种物质的漂白原理与其它不同的是 ( )
A.次氯酸 B.过氧化氢 C.三氧化硫 D.臭氧
28.(8分)为确定某铝热剂(含四氧化三铁和铝)的组成,分别进行下列实验。
(1)若取38g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为11.2L ,该反应的离子方程式为 ;样品中铝的质量是 g。
(2)若取38g样品将其点燃,恰好完全反应,四氧化三铁与铝的质量比是 。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为aL,该气体与(1)中所得气体的体积比等于 。
27.(12分)A、B、C是中学常见的无机物,且各由两种元素组成;甲、乙、丙是三种常见的单质;这些化合物和单质间存在如图所示的转化关系(这些转化都不需要使用催化剂)。
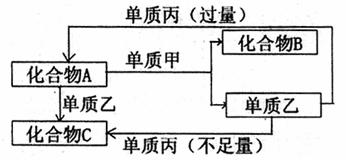
请回答下列问题:
(1)若甲在转化中是还原剂,乙是常见非金属固态单质,且甲、乙、丙都是由短周期元素组成,则:甲 ;乙 ;丙 (填化学式);化合物A的电子式 。A与甲反应的化学方程式为 。
(2)若甲在转化中为氧化剂,是常见非金属气态单质,丙是常见金属,甲、乙、丙中只有甲由短周期元素组成,乙的组成元素与甲的组成元素同主族、与丙的组成元素同周期,乙有强氧化性。且反应均在通常条件下的溶液中进行,则:
① A与乙反应的离子方程式为 ;
②当A与甲的物质的量之比为 时,A与甲恰好完全反应,且符合图中所示的转化关系,则反应的离子方程式为
。
时,A与甲恰好完全反应,且符合图中所示的转化关系,则反应的离子方程式为
。
③0.1mol的单质甲与50mL1.5 mol · L – 1化合物A的溶液反应,则化合物A中被氧化的阴、阳离子的物质的量之比是 。
26.(18分)
(1)实验室利用图1装置进行中和热的测定。
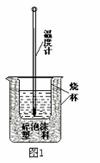
①该图中有两处仪器未画出,它们是 ,
;
②如果用0.5 mol · L – 1的盐酸和氢氧化钠固体进行实验,则所测出的“中和热”将
(填“偏大”、“偏小”、“不变”);原因是 。
(2)用图2装置进行测定硫酸亚铁晶体(FeSO4·nH2O)中结晶水含量的实验(图中半透膜可让气体通过又可防止固体粉末进入导管)。
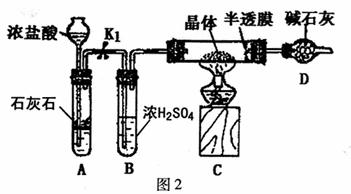
请回答下列问题:
①碱石灰的作用是 。
②假设已检验好装置的气密性,将m1g晶体置于C装置的硬质玻璃管中, 并称得D装置的质量为ag。依据上图设计实验步骤,并填写在横线上:
第一步:打开K1 ,让装置A中产生的气体充满整个装置;
此步实验操作的目的是: ;
第二步: ;
第三步:熄灭酒精灯,停止加热;
第四步: ;
第五步:称量C装置中固体的质量为m2g,D装置的质量为bg。
③根据实验结果,计算硫酸亚铁晶体中结晶水的n值为 。
24.(13分)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液c;A、B分别是两块电极板,通过导线与直流电源相连。

(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U型管两边各滴入几滴酚酞试液,试判断①a是 极(填“正”或“负”),B是 极(填“阴”或“阳”);
②A电极上的电极反应式为 ,
B电极上的电极反应式为 ;
③检验A电极产物的方法是 。
(2)如用电解法精炼粗铜,电解液c选用CuSO4溶液,则
①A电极的材料是 ,电极反应式为 ;
②B电极的材料是 ,电极反应式为 。
(3)用惰性电极电解CuSO4溶液。若阴极上析出Cu的质量为3.2g,则阳极上产生气体在标准状况下的体积为 ;常温下,若将电解后的溶液稀释至1 L,则溶液的pH约为 。
25(19分).已知溴乙烷跟氰化钠反应后再水解可以得到丙酸:
|
|
||||

 CH3CH2Br
CH3CH2CN
CH3CH2COOH
CH3CH2Br
CH3CH2CN
CH3CH2COOH
产物分子比原化合物分子多了一个碳原子,增长了碳链。下图为某单烯烃反应的转化关系图,其中2分子B可以在浓硫酸加热的条件下,生成六元环醚(C4H8O2);E为链状高分子化合物。
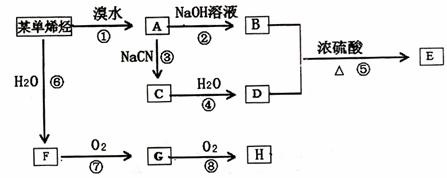
请回答下列问题:
(1)化合物F、D中含有的官能团的名称分别是 ; 。
(2)反应类型:② ; ⑥ 。
(3)化合物E的结构简式是 。
(4)写出F和H反应的化学方程式 ;
(5)简述检验G分子中含有的官能团的实验步骤:
;
写出G参与反应的化学方程式 。
(6)H可以发生酯化反应生成乙酸异丁酯。某有机物能发生银镜反应,与乙酸异丁酯互为同分异构体。该有机物在酸性条件下水解成M、N,N在铜催化作用下能氧化成I, I不能发生银镜反应。则该有机物可能的结构有 种,写出符合此条件的有机物的结构简式(两种即可)
;
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com